สารที่ประกอบด้วยไนโตรเจนที่มีคุณสมบัติเป็นด่างเรียกว่า ปฏิกิริยากับกรด
 การจำแนกประเภทสารประกอบกลุ่มนี้ประกอบด้วยหลายประเภท: เอมีน เอไมด์ อิไมด์ สารประกอบเอโซ สารประกอบไดโซ กรดอะมิโน สารประกอบไนโตร สารประกอบไนโตรโซ
การจำแนกประเภทสารประกอบกลุ่มนี้ประกอบด้วยหลายประเภท: เอมีน เอไมด์ อิไมด์ สารประกอบเอโซ สารประกอบไดโซ กรดอะมิโน สารประกอบไนโตร สารประกอบไนโตรโซ
 เอมีน เอมีนถือได้ว่าเป็นอนุพันธ์ของแอมโมเนีย เอมีนเรียกว่า สารประกอบอินทรีย์ซึ่งได้มาจากการแทนที่อะตอมไฮโดรเจนในแอมโมเนียด้วยอนุมูลไฮโดรคาร์บอน
เอมีน เอมีนถือได้ว่าเป็นอนุพันธ์ของแอมโมเนีย เอมีนเรียกว่า สารประกอบอินทรีย์ซึ่งได้มาจากการแทนที่อะตอมไฮโดรเจนในแอมโมเนียด้วยอนุมูลไฮโดรคาร์บอน
 o การจำแนกประเภท เอมีนแบ่งออกเป็น: ประถมศึกษา มัธยมศึกษาตอนปลาย
o การจำแนกประเภท เอมีนแบ่งออกเป็น: ประถมศึกษา มัธยมศึกษาตอนปลาย
 เอมีนแบ่งออกเป็น: § ขีดจำกัด; § ไม่ จำกัด; § อะโรมาติก ขึ้นอยู่กับจำนวนกลุ่มอะมิโน เอมีนจะถูกแบ่งออกเป็น: § โมโนเอมีน; § ไดเอมีน; § โพลีเอมีน
เอมีนแบ่งออกเป็น: § ขีดจำกัด; § ไม่ จำกัด; § อะโรมาติก ขึ้นอยู่กับจำนวนกลุ่มอะมิโน เอมีนจะถูกแบ่งออกเป็น: § โมโนเอมีน; § ไดเอมีน; § โพลีเอมีน
 o ระบบการตั้งชื่อสากล ชื่อของเอมีนประกอบด้วยคำสองคำ: ชื่อของอนุมูลไฮโดรคาร์บอนตามระบบการตั้งชื่อที่รุนแรงและคำว่า "เอมีน" มีเหตุผล. ใช้เพื่อสร้างชื่อของเอมีนปฐมภูมิเท่านั้น ขึ้นอยู่กับชื่อของไฮโดรคาร์บอนและคำนำหน้า "อะมิโน-" ที่ด้านหน้าซึ่งระบุตำแหน่งของหมู่อะมิโนด้วยตัวเลข บางครั้งใช้คำต่อท้าย “เอมีน” แทนคำนำหน้า
o ระบบการตั้งชื่อสากล ชื่อของเอมีนประกอบด้วยคำสองคำ: ชื่อของอนุมูลไฮโดรคาร์บอนตามระบบการตั้งชื่อที่รุนแรงและคำว่า "เอมีน" มีเหตุผล. ใช้เพื่อสร้างชื่อของเอมีนปฐมภูมิเท่านั้น ขึ้นอยู่กับชื่อของไฮโดรคาร์บอนและคำนำหน้า "อะมิโน-" ที่ด้านหน้าซึ่งระบุตำแหน่งของหมู่อะมิโนด้วยตัวเลข บางครั้งใช้คำต่อท้าย “เอมีน” แทนคำนำหน้า
 เอมีนปฐมภูมิ Methylamine Aminomethane Metalamine Ethylamine Aminoethane Propylamine 1 -aminopropane Isopropylamine 2 -aminopropane Propylamine-2 วินาที โพรพิลามีน บิวทิลามีน 1-อะมิโนบิวเทน
เอมีนปฐมภูมิ Methylamine Aminomethane Metalamine Ethylamine Aminoethane Propylamine 1 -aminopropane Isopropylamine 2 -aminopropane Propylamine-2 วินาที โพรพิลามีน บิวทิลามีน 1-อะมิโนบิวเทน
 ฉธบ. บิวทิลามีน 2 -อะมิโนบิวเทน ไอโซบิวทิลามีน 2 -เมทิล-1 -อะมิโนโพรเพน อะมิโนไอโซบิวเทน Tert บิวทิลามีน 2-เมทิล-2-อะมิโนโพรเพน 2-เมทิลโพรพิลามีน-2 เอมีนรอง ไดเมทิลลามีน เมทิลเอทิลเอมีน
ฉธบ. บิวทิลามีน 2 -อะมิโนบิวเทน ไอโซบิวทิลามีน 2 -เมทิล-1 -อะมิโนโพรเพน อะมิโนไอโซบิวเทน Tert บิวทิลามีน 2-เมทิล-2-อะมิโนโพรเพน 2-เมทิลโพรพิลามีน-2 เอมีนรอง ไดเมทิลลามีน เมทิลเอทิลเอมีน


 o คุณสมบัติทางกายภาพ เมทิลเอมีน, ไดเมทิลลามีน, ไตรเมทิลลามีน เป็นก๊าซ เอมีนส่วนล่างที่เหลือเป็นของเหลว เอมีนที่สูงขึ้นคือของแข็ง เอมีนก็มี กลิ่นอันไม่พึงประสงค์“ แฮร์ริ่งน้ำเกลือ” ซึ่งเด่นชัดกว่าในอันที่ต่ำกว่าและอ่อนแอกว่า (หรือขาดหายไป) ในอันที่สูงกว่า เอมีนส่วนล่าง (ตัวแทนกลุ่มแรก) ค่อนข้างละลายได้ในน้ำ (เช่นแอมโมเนีย) สารละลายของพวกมันมีปฏิกิริยาพื้นฐานของตัวกลาง
o คุณสมบัติทางกายภาพ เมทิลเอมีน, ไดเมทิลลามีน, ไตรเมทิลลามีน เป็นก๊าซ เอมีนส่วนล่างที่เหลือเป็นของเหลว เอมีนที่สูงขึ้นคือของแข็ง เอมีนก็มี กลิ่นอันไม่พึงประสงค์“ แฮร์ริ่งน้ำเกลือ” ซึ่งเด่นชัดกว่าในอันที่ต่ำกว่าและอ่อนแอกว่า (หรือขาดหายไป) ในอันที่สูงกว่า เอมีนส่วนล่าง (ตัวแทนกลุ่มแรก) ค่อนข้างละลายได้ในน้ำ (เช่นแอมโมเนีย) สารละลายของพวกมันมีปฏิกิริยาพื้นฐานของตัวกลาง
 o วิธีการผลิต ในปี 1850 นักวิทยาศาสตร์ชาวเยอรมัน Hoffmann ได้รับเอมีนเป็นครั้งแรกอันเป็นผลมาจากปฏิกิริยาทางเคมีระหว่างไฮโดรคาร์บอนที่เติมฮาโลเจนกับแอมโมเนียที่มากเกินไป จำเป็นต้องมีแอมโมเนียที่มากเกินไปเพื่อให้ได้เอมีนบริสุทธิ์ หากไม่มีแอมโมเนีย จะเกิดส่วนผสมขึ้นเสมอ
o วิธีการผลิต ในปี 1850 นักวิทยาศาสตร์ชาวเยอรมัน Hoffmann ได้รับเอมีนเป็นครั้งแรกอันเป็นผลมาจากปฏิกิริยาทางเคมีระหว่างไฮโดรคาร์บอนที่เติมฮาโลเจนกับแอมโมเนียที่มากเกินไป จำเป็นต้องมีแอมโมเนียที่มากเกินไปเพื่อให้ได้เอมีนบริสุทธิ์ หากไม่มีแอมโมเนีย จะเกิดส่วนผสมขึ้นเสมอ

 เอมีนปฐมภูมิมีฤทธิ์ทางชีวภาพมากที่สุด ได้มาจากการสลายตัวของกรดเอไมด์ (การจัดเรียงใหม่ของฮอฟฟ์แมนน์) กรดโพรพิโอนิกเอไมด์ วิธีนี้ใช้กันอย่างแพร่หลายในห้องปฏิบัติการ
เอมีนปฐมภูมิมีฤทธิ์ทางชีวภาพมากที่สุด ได้มาจากการสลายตัวของกรดเอไมด์ (การจัดเรียงใหม่ของฮอฟฟ์แมนน์) กรดโพรพิโอนิกเอไมด์ วิธีนี้ใช้กันอย่างแพร่หลายในห้องปฏิบัติการ
 ในอุตสาหกรรม เอมีนปฐมภูมิได้มาจากการลดสารประกอบไนโตรและกรดไนไตรล์ ไนโตรอีเทน กรดโพรพิโอนิก ไนไตรล์ เอทิลลามีน โพรพิลามีน
ในอุตสาหกรรม เอมีนปฐมภูมิได้มาจากการลดสารประกอบไนโตรและกรดไนไตรล์ ไนโตรอีเทน กรดโพรพิโอนิก ไนไตรล์ เอทิลลามีน โพรพิลามีน






 ปฏิกิริยากับกรดไนตรัส เมื่อเอมีนปฐมภูมิทำปฏิกิริยากับกรดไนตรัส จะเกิดแอลกอฮอล์ปฐมภูมิ
ปฏิกิริยากับกรดไนตรัส เมื่อเอมีนปฐมภูมิทำปฏิกิริยากับกรดไนตรัส จะเกิดแอลกอฮอล์ปฐมภูมิ
 เอมีนทุติยภูมิทำปฏิกิริยากับกรดไนตรัสเพื่อสร้างไนโตรซามีน (สารประกอบสีเหลืองส้ม)
เอมีนทุติยภูมิทำปฏิกิริยากับกรดไนตรัสเพื่อสร้างไนโตรซามีน (สารประกอบสีเหลืองส้ม)




 ออกซิเดชัน. เป็นเรื่องยากและผลลัพธ์ขึ้นอยู่กับโครงสร้าง การเกิดออกซิเดชันของเอมีนปฐมภูมิทำให้เกิดสารประกอบไนโตร
ออกซิเดชัน. เป็นเรื่องยากและผลลัพธ์ขึ้นอยู่กับโครงสร้าง การเกิดออกซิเดชันของเอมีนปฐมภูมิทำให้เกิดสารประกอบไนโตร



 เหล่านี้เป็นสารประกอบในโมเลกุลที่หมู่อะมิโนเชื่อมโยงกับวงแหวนเบนซีน ตัวแทนและบรรพบุรุษที่ง่ายที่สุดของสีย้อมสวรรค์คือ
เหล่านี้เป็นสารประกอบในโมเลกุลที่หมู่อะมิโนเชื่อมโยงกับวงแหวนเบนซีน ตัวแทนและบรรพบุรุษที่ง่ายที่สุดของสีย้อมสวรรค์คือ

 โอ คุณสมบัติทางกายภาพ สวรรค์เป็นของเหลวไม่มีสีที่เปลี่ยนเป็นสีน้ำตาลอย่างรวดเร็วในอากาศ ละลายได้ไม่ดีในน้ำ
โอ คุณสมบัติทางกายภาพ สวรรค์เป็นของเหลวไม่มีสีที่เปลี่ยนเป็นสีน้ำตาลอย่างรวดเร็วในอากาศ ละลายได้ไม่ดีในน้ำ
 โอ คุณสมบัติทางเคมีเกิดจากทั้งหมู่อะมิโนและวงแหวนเบนซีน หมู่อะมิโนเป็นองค์ประกอบทดแทนที่ให้อิเล็กตรอน และคุณสมบัติของอะนิลีนเนื่องจากวงแหวนเบนซีนมีดังนี้:
โอ คุณสมบัติทางเคมีเกิดจากทั้งหมู่อะมิโนและวงแหวนเบนซีน หมู่อะมิโนเป็นองค์ประกอบทดแทนที่ให้อิเล็กตรอน และคุณสมบัติของอะนิลีนเนื่องจากวงแหวนเบนซีนมีดังนี้:


 การโต้ตอบกับแอลกอฮอล์ – เฉพาะเจาะจง คุณสมบัติทางเคมีหมู่อะมิโนเนื่องจากสัมผัสโดยตรงกับวงแหวนเบนซีน
การโต้ตอบกับแอลกอฮอล์ – เฉพาะเจาะจง คุณสมบัติทางเคมีหมู่อะมิโนเนื่องจากสัมผัสโดยตรงกับวงแหวนเบนซีน



 ยูเรียเป็นเอไมด์ที่สมบูรณ์ของกรดคาร์บอนิก กระจายอยู่ทั่วไปในธรรมชาติ มันเป็นผลิตภัณฑ์ขั้นสุดท้ายของการเผาผลาญโปรตีน ภายใต้สภาวะปกติ ยูเรียเป็นสารผลึกแข็งที่ละลายที่อุณหภูมิ 133 C สามารถละลายได้ดีในขั้วไฟฟ้าและไม่ละลายอย่างแน่นอนในตัวทำละลายที่ไม่มีขั้ว มันมีคุณสมบัติพื้นฐานที่อ่อนแอ แต่มีความเด่นชัดน้อยกว่าเอมีนเนื่องจากกลุ่มคาร์บอนิล
ยูเรียเป็นเอไมด์ที่สมบูรณ์ของกรดคาร์บอนิก กระจายอยู่ทั่วไปในธรรมชาติ มันเป็นผลิตภัณฑ์ขั้นสุดท้ายของการเผาผลาญโปรตีน ภายใต้สภาวะปกติ ยูเรียเป็นสารผลึกแข็งที่ละลายที่อุณหภูมิ 133 C สามารถละลายได้ดีในขั้วไฟฟ้าและไม่ละลายอย่างแน่นอนในตัวทำละลายที่ไม่มีขั้ว มันมีคุณสมบัติพื้นฐานที่อ่อนแอ แต่มีความเด่นชัดน้อยกว่าเอมีนเนื่องจากกลุ่มคาร์บอนิล

 การได้รับยูเรีย ในอุตสาหกรรม ยูเรียถูกผลิตขึ้นโดยวิธีการดังต่อไปนี้ โดยการทำปฏิกิริยากรดคาร์บอนิกเฮไลด์โดยสมบูรณ์กับแอมโมเนีย
การได้รับยูเรีย ในอุตสาหกรรม ยูเรียถูกผลิตขึ้นโดยวิธีการดังต่อไปนี้ โดยการทำปฏิกิริยากรดคาร์บอนิกเฮไลด์โดยสมบูรณ์กับแอมโมเนีย








 ไบยูเรตเป็นสารประกอบอินทรีย์ที่ง่ายที่สุดที่มีพันธะเปปไทด์ พันธะเปปไทด์เป็นพันธะพื้นฐานของตัวโปรตีนตามธรรมชาติทั้งหมด ปฏิกิริยาของไบยูเรตกับคอปเปอร์ (II) ไฮดรอกไซด์เป็นปฏิกิริยาเชิงคุณภาพสำหรับโปรตีน
ไบยูเรตเป็นสารประกอบอินทรีย์ที่ง่ายที่สุดที่มีพันธะเปปไทด์ พันธะเปปไทด์เป็นพันธะพื้นฐานของตัวโปรตีนตามธรรมชาติทั้งหมด ปฏิกิริยาของไบยูเรตกับคอปเปอร์ (II) ไฮดรอกไซด์เป็นปฏิกิริยาเชิงคุณภาพสำหรับโปรตีน


 กรดอะมิโนเป็นอนุพันธ์ของกรดคาร์บอกซิลิกที่สามารถได้รับโดยการแทนที่อะตอมไฮโดรเจนตั้งแต่หนึ่งอะตอมขึ้นไปในอนุมูลของกรด
กรดอะมิโนเป็นอนุพันธ์ของกรดคาร์บอกซิลิกที่สามารถได้รับโดยการแทนที่อะตอมไฮโดรเจนตั้งแต่หนึ่งอะตอมขึ้นไปในอนุมูลของกรด
 o การจำแนกประเภท ขึ้นอยู่กับจำนวนหมู่คาร์บอกซิล: Monobasic Dibasic Polybasic
o การจำแนกประเภท ขึ้นอยู่กับจำนวนหมู่คาร์บอกซิล: Monobasic Dibasic Polybasic
 ขึ้นอยู่กับจำนวนหมู่อะมิโน: กรดโมโนอะมิโน, กรดไดอะมิโน, กรดไตรอะมิโน ขึ้นอยู่กับโครงสร้างของอนุมูล: วงจรโซ่เปิด
ขึ้นอยู่กับจำนวนหมู่อะมิโน: กรดโมโนอะมิโน, กรดไดอะมิโน, กรดไตรอะมิโน ขึ้นอยู่กับโครงสร้างของอนุมูล: วงจรโซ่เปิด
 o ระบบการตั้งชื่อสากล: กฎสำหรับการสร้างชื่อจะเหมือนกับกรดคาร์บอกซิลิกโดยมีเพียงการมีอยู่ ปริมาณ และตำแหน่งของหมู่อะมิโนที่ระบุไว้ในคำนำหน้าเท่านั้น เหตุผล: ตำแหน่งของกลุ่มอะมิโนระบุด้วยตัวอักษรของอักษรกรีก + คำว่า "อะมิโน" + ชื่อ กรดคาร์บอกซิลิกตามระบบการตั้งชื่อที่มีเหตุผล
o ระบบการตั้งชื่อสากล: กฎสำหรับการสร้างชื่อจะเหมือนกับกรดคาร์บอกซิลิกโดยมีเพียงการมีอยู่ ปริมาณ และตำแหน่งของหมู่อะมิโนที่ระบุไว้ในคำนำหน้าเท่านั้น เหตุผล: ตำแหน่งของกลุ่มอะมิโนระบุด้วยตัวอักษรของอักษรกรีก + คำว่า "อะมิโน" + ชื่อ กรดคาร์บอกซิลิกตามระบบการตั้งชื่อที่มีเหตุผล
 o ISOMERITY ไอโซเมอร์ริซึมของตำแหน่งของหมู่อะมิโนสัมพันธ์กับหมู่คาร์บอกซิล มี α-, β-, γ-, δ-, ε- เป็นต้น
o ISOMERITY ไอโซเมอร์ริซึมของตำแหน่งของหมู่อะมิโนสัมพันธ์กับหมู่คาร์บอกซิล มี α-, β-, γ-, δ-, ε- เป็นต้น



 o คุณสมบัติทางกายภาพ กรดอะมิโนเป็นสารผลึกไม่มีสีและมีจุดหลอมเหลวสูง อย่าบิน. ละลายไปกับการสลายตัว ละลายได้ดีในน้ำและละลายได้ไม่ดีในตัวทำละลายอินทรีย์ พวกเขามีกิจกรรมทางแสง
o คุณสมบัติทางกายภาพ กรดอะมิโนเป็นสารผลึกไม่มีสีและมีจุดหลอมเหลวสูง อย่าบิน. ละลายไปกับการสลายตัว ละลายได้ดีในน้ำและละลายได้ไม่ดีในตัวทำละลายอินทรีย์ พวกเขามีกิจกรรมทางแสง

 ซีรีย์โฮโมโลจิคอล 2 -อะมิโนอีเทน α-อะมิโนอะซิติกไกลซีน 2 -อะมิโนโพรเพน α-อะมิโนโพรพิโอนิก α-อะลานีน 3 -อะมิโนโพรเพน β-อะมิโนโพรพิโอนิก β-อะลานีน 2 -อะมิโนบิวเทน α-อะมิโนบิวทีริก 3 -อะมิโนบิวเทน β-อะมิโนบิวทีริก 4 -อะมิโนบิวเทน γ-อะมิโนบิวทีริก
ซีรีย์โฮโมโลจิคอล 2 -อะมิโนอีเทน α-อะมิโนอะซิติกไกลซีน 2 -อะมิโนโพรเพน α-อะมิโนโพรพิโอนิก α-อะลานีน 3 -อะมิโนโพรเพน β-อะมิโนโพรพิโอนิก β-อะลานีน 2 -อะมิโนบิวเทน α-อะมิโนบิวทีริก 3 -อะมิโนบิวเทน β-อะมิโนบิวทีริก 4 -อะมิโนบิวเทน γ-อะมิโนบิวทีริก





 คุณสมบัติเฉพาะของกรดอะมิโน สัมพันธ์กับการให้ความร้อนของกรด α-อะมิโน ในกรณีที่ไม่มีกรดแร่
คุณสมบัติเฉพาะของกรดอะมิโน สัมพันธ์กับการให้ความร้อนของกรด α-อะมิโน ในกรณีที่ไม่มีกรดแร่





 กรดอะมิโน Dibasic สามารถสร้างเกลือภายในได้ ทั้งสองพบได้ในผลิตภัณฑ์จากการไฮโดรไลซิสของโปรตีน กรดแอสปาร์ติกพบได้ในรูปแบบอิสระในสิ่งมีชีวิตในสัตว์และพืช กำลังเล่น บทบาทสำคัญในการเผาผลาญไนโตรเจน แบบฟอร์มเอไมด์ - แอสปาร์จีน กรดกลูตามิกใช้ในการรักษาความผิดปกติทางจิต แบบฟอร์มเอไมด์ - กลูตามีน
กรดอะมิโน Dibasic สามารถสร้างเกลือภายในได้ ทั้งสองพบได้ในผลิตภัณฑ์จากการไฮโดรไลซิสของโปรตีน กรดแอสปาร์ติกพบได้ในรูปแบบอิสระในสิ่งมีชีวิตในสัตว์และพืช กำลังเล่น บทบาทสำคัญในการเผาผลาญไนโตรเจน แบบฟอร์มเอไมด์ - แอสปาร์จีน กรดกลูตามิกใช้ในการรักษาความผิดปกติทางจิต แบบฟอร์มเอไมด์ - กลูตามีน


Src="https://present5.com/presentation/1/206975869_437124838.pdf-img/206975869_437124838.pdf-81.jpg" alt="คุณสมบัติทางเคมี การทำปฏิกิริยากับน้ำ (ในสารละลายที่เป็นน้ำ p. H>7 )"> ХИМИЧЕСКИЕ СВОЙСТВА Взаимодействие с водой (в водных растворах p. H>7)!}

 กรดα-amino เกี่ยวข้องกับการสังเคราะห์โปรตีน ร่างกายโปรตีนยังรวมถึงกรดอะมิโนที่นอกเหนือจากหมู่อะมิโนแล้ว ยังมีหมู่ฟังก์ชันอื่นๆ ด้วย ตามความสำคัญต่อร่างกาย กรดอะมิโนทั้งหมดแบ่งออกเป็น: § ทดแทนได้ (สังเคราะห์ในร่างกาย) § ไม่สามารถทดแทนได้ (เติมด้วยอาหารเท่านั้น)
กรดα-amino เกี่ยวข้องกับการสังเคราะห์โปรตีน ร่างกายโปรตีนยังรวมถึงกรดอะมิโนที่นอกเหนือจากหมู่อะมิโนแล้ว ยังมีหมู่ฟังก์ชันอื่นๆ ด้วย ตามความสำคัญต่อร่างกาย กรดอะมิโนทั้งหมดแบ่งออกเป็น: § ทดแทนได้ (สังเคราะห์ในร่างกาย) § ไม่สามารถทดแทนได้ (เติมด้วยอาหารเท่านั้น)
 สูตรการตั้งชื่อ ตามระบบการตั้งชื่อแบบอนุสัญญาเล็กๆ น้อยๆ เกี่ยวกับ. α-aminoacetic Glycine gly α-aminopropionic Alanine Ala α-aminoisovaleric Valine val α-aminoisocaproic Leucine leu วินาที บิวทิล-αอะมิโนอะซิติก ไอโซลิวซีน อิล
สูตรการตั้งชื่อ ตามระบบการตั้งชื่อแบบอนุสัญญาเล็กๆ น้อยๆ เกี่ยวกับ. α-aminoacetic Glycine gly α-aminopropionic Alanine Ala α-aminoisovaleric Valine val α-aminoisocaproic Leucine leu วินาที บิวทิล-αอะมิโนอะซิติก ไอโซลิวซีน อิล

 α, εdiamine Apric acid ไลซีน lys α-amino-δ guanidol อาร์จินีน lerianic ARG α-amino-βoxypropionovy serine serine α-aminoβoxybutyric threonine tre β-thio-αaminoprop ionic cysteine cis
α, εdiamine Apric acid ไลซีน lys α-amino-δ guanidol อาร์จินีน lerianic ARG α-amino-βoxypropionovy serine serine α-aminoβoxybutyric threonine tre β-thio-αaminoprop ionic cysteine cis
 ซีสตีน α-amino-γ-methionine methylthiome asyl α-amino-βphenylpropionic acid ฟีนิลอะลีน β-ptyrosine oxyphenylαaminopropanoic acid cin met phen tyre
ซีสตีน α-amino-γ-methionine methylthiome asyl α-amino-βphenylpropionic acid ฟีนิลอะลีน β-ptyrosine oxyphenylαaminopropanoic acid cin met phen tyre

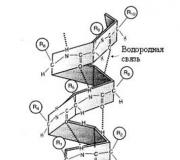
 โปรตีน โปรตีนหรือสารโปรตีนเป็นสารประกอบอินทรีย์โมเลกุลสูงซึ่งโมเลกุลสร้างขึ้นจากสารตกค้างของกรด α-อะมิโนที่เชื่อมโยงกันด้วยพันธะเปปไทด์ จำนวนหลังสามารถผันผวนอย่างมากและบางครั้งก็สูงถึงหลายพัน โครงสร้างของโปรตีนมีความซับซ้อนมาก สายเปปไทด์แต่ละสายหรือแต่ละส่วนสามารถเชื่อมโยงถึงกันด้วยพันธะไดซัลไฟด์ เกลือ หรือไฮโดรเจน พันธะเกลือถูกสร้างขึ้นระหว่างหมู่อะมิโนอิสระ (ตัวอย่างเช่น หมู่เทอร์มินัลอะมิโนที่อยู่ที่ปลายด้านหนึ่งของสายโพลีเปปไทด์หรือหมู่ ε-อะมิโนของไลซีน) และหมู่คาร์บอกซิลอิสระ (หมู่คาร์บอกซิลส่วนปลายของสายหรือหมู่คาร์บอกซิลอิสระ ของกรดอะมิโน dibasic); พันธะไฮโดรเจนสามารถเกิดขึ้นได้ระหว่างอะตอมออกซิเจนของกลุ่มคาร์บอนิลและอะตอมไฮโดรเจนของกลุ่มอะมิโน เช่นเดียวกับกลุ่มไฮดรอกโซของกรดอะมิโนไฮดรอกซีและออกซิเจนของกลุ่มเปปไทด์
โปรตีน โปรตีนหรือสารโปรตีนเป็นสารประกอบอินทรีย์โมเลกุลสูงซึ่งโมเลกุลสร้างขึ้นจากสารตกค้างของกรด α-อะมิโนที่เชื่อมโยงกันด้วยพันธะเปปไทด์ จำนวนหลังสามารถผันผวนอย่างมากและบางครั้งก็สูงถึงหลายพัน โครงสร้างของโปรตีนมีความซับซ้อนมาก สายเปปไทด์แต่ละสายหรือแต่ละส่วนสามารถเชื่อมโยงถึงกันด้วยพันธะไดซัลไฟด์ เกลือ หรือไฮโดรเจน พันธะเกลือถูกสร้างขึ้นระหว่างหมู่อะมิโนอิสระ (ตัวอย่างเช่น หมู่เทอร์มินัลอะมิโนที่อยู่ที่ปลายด้านหนึ่งของสายโพลีเปปไทด์หรือหมู่ ε-อะมิโนของไลซีน) และหมู่คาร์บอกซิลอิสระ (หมู่คาร์บอกซิลส่วนปลายของสายหรือหมู่คาร์บอกซิลอิสระ ของกรดอะมิโน dibasic); พันธะไฮโดรเจนสามารถเกิดขึ้นได้ระหว่างอะตอมออกซิเจนของกลุ่มคาร์บอนิลและอะตอมไฮโดรเจนของกลุ่มอะมิโน เช่นเดียวกับกลุ่มไฮดรอกโซของกรดอะมิโนไฮดรอกซีและออกซิเจนของกลุ่มเปปไทด์
 โปรตีน มีโครงสร้างโมเลกุลโปรตีนในระดับปฐมภูมิ ทุติยภูมิ ตติยภูมิ และควอเทอร์นารี โปรตีนทั้งหมดไม่ว่าพวกมันจะอยู่ในกลุ่มใดก็ตามและทำหน้าที่อะไรก็ตาม ถูกสร้างขึ้นจากกรดอะมิโนชุดที่ค่อนข้างเล็ก (ปกติ 20 ตัว) ซึ่งอยู่ในลำดับที่แตกต่างออกไป แต่ถูกกำหนดไว้อย่างเข้มงวดเสมอสำหรับโปรตีนประเภทหนึ่งๆ โปรตีนแบ่งออกเป็นโปรตีนและโปรตีน Ø โปรตีนเป็นโปรตีนอย่างง่ายที่ประกอบด้วยกรดอะมิโนตกค้างเท่านั้น ü อัลบูมิน – มีน้ำหนักโมเลกุลค่อนข้างเล็ก ละลายน้ำได้สูง และจับตัวเป็นก้อนเมื่อถูกความร้อน
โปรตีน มีโครงสร้างโมเลกุลโปรตีนในระดับปฐมภูมิ ทุติยภูมิ ตติยภูมิ และควอเทอร์นารี โปรตีนทั้งหมดไม่ว่าพวกมันจะอยู่ในกลุ่มใดก็ตามและทำหน้าที่อะไรก็ตาม ถูกสร้างขึ้นจากกรดอะมิโนชุดที่ค่อนข้างเล็ก (ปกติ 20 ตัว) ซึ่งอยู่ในลำดับที่แตกต่างออกไป แต่ถูกกำหนดไว้อย่างเข้มงวดเสมอสำหรับโปรตีนประเภทหนึ่งๆ โปรตีนแบ่งออกเป็นโปรตีนและโปรตีน Ø โปรตีนเป็นโปรตีนอย่างง่ายที่ประกอบด้วยกรดอะมิโนตกค้างเท่านั้น ü อัลบูมิน – มีน้ำหนักโมเลกุลค่อนข้างเล็ก ละลายน้ำได้สูง และจับตัวเป็นก้อนเมื่อถูกความร้อน
 โปรตีน ü โกลบูลิน – ไม่ละลายใน น้ำสะอาดแต่ละลายได้ในสารละลาย Na 10% ที่อบอุ่น Cl. ü โปรลามินละลายได้ในน้ำเล็กน้อย แต่ละลายได้ในเอทิลแอลกอฮอล์ในน้ำ 60–80% ü Glutelins ละลายได้ในอัลคาไล 0.2% เท่านั้น ü Protamines – ไม่มีกำมะถันเลย ü โปรตีนออยด์เป็นโปรตีนที่ไม่ละลายน้ำ ü ฟอสโฟโปรตีน – มีกรดฟอสฟอริก (เคซีน)
โปรตีน ü โกลบูลิน – ไม่ละลายใน น้ำสะอาดแต่ละลายได้ในสารละลาย Na 10% ที่อบอุ่น Cl. ü โปรลามินละลายได้ในน้ำเล็กน้อย แต่ละลายได้ในเอทิลแอลกอฮอล์ในน้ำ 60–80% ü Glutelins ละลายได้ในอัลคาไล 0.2% เท่านั้น ü Protamines – ไม่มีกำมะถันเลย ü โปรตีนออยด์เป็นโปรตีนที่ไม่ละลายน้ำ ü ฟอสโฟโปรตีน – มีกรดฟอสฟอริก (เคซีน)
 โปรตีน Ø โปรตีนเป็นโปรตีนเชิงซ้อน ซึ่งรวมถึงคาร์โบไฮเดรต ไขมัน สารประกอบเฮเทอโรไซคลิก กรดนิวคลีอิก และกรดฟอสฟอริก พร้อมด้วยกรดอะมิโน ü ไลโปโปรตีน - ไฮโดรไลซ์เป็นโปรตีนและไขมันอย่างง่าย (เมล็ดคลอโรฟิลล์, โปรโตพลาสซึมของเซลล์) ü ไกลโคโปรตีน – ไฮโดรไลซ์เป็นโปรตีนเชิงเดี่ยวและคาร์โบไฮเดรตน้ำหนักโมเลกุลสูง (สารคัดหลั่งของสัตว์) ü โครโมโปรตีน - ไฮโดรไลซ์เป็นโปรตีนเชิงเดี่ยวและสีย้อม (เฮโมโกลบิน) ü นิวคลีโอโปรตีน - ไฮโดรไลซ์เป็นโปรตีนเชิงเดี่ยว (โดยปกติคือโปรทามีน) และกรดนิวคลีอิก
โปรตีน Ø โปรตีนเป็นโปรตีนเชิงซ้อน ซึ่งรวมถึงคาร์โบไฮเดรต ไขมัน สารประกอบเฮเทอโรไซคลิก กรดนิวคลีอิก และกรดฟอสฟอริก พร้อมด้วยกรดอะมิโน ü ไลโปโปรตีน - ไฮโดรไลซ์เป็นโปรตีนและไขมันอย่างง่าย (เมล็ดคลอโรฟิลล์, โปรโตพลาสซึมของเซลล์) ü ไกลโคโปรตีน – ไฮโดรไลซ์เป็นโปรตีนเชิงเดี่ยวและคาร์โบไฮเดรตน้ำหนักโมเลกุลสูง (สารคัดหลั่งของสัตว์) ü โครโมโปรตีน - ไฮโดรไลซ์เป็นโปรตีนเชิงเดี่ยวและสีย้อม (เฮโมโกลบิน) ü นิวคลีโอโปรตีน - ไฮโดรไลซ์เป็นโปรตีนเชิงเดี่ยว (โดยปกติคือโปรทามีน) และกรดนิวคลีอิก
สารประกอบไนโตร สารประกอบไนโตรเป็นสารอินทรีย์ที่มีโมเลกุลประกอบด้วยกลุ่มไนโตร - NO 2 ที่อะตอมของคาร์บอน
ถือได้ว่าเป็นอนุพันธ์ของไฮโดรคาร์บอนซึ่งได้มาจากการแทนที่อะตอมไฮโดรเจนด้วยหมู่ไนโตร ขึ้นอยู่กับจำนวนหมู่ไนโตรที่พวกเขาแยกแยะได้ สารประกอบโมโน ได และโพลีไนโตร
ชื่อของสารประกอบไนโตร มาจากชื่อของไฮโดรคาร์บอนดั้งเดิมที่มีการเติมคำนำหน้า ไนโตร:
สูตรทั่วไปของสารประกอบเหล่านี้คือ R-NO 2
บทนำสู่ อินทรียฺวัตถุเรียกว่า หมู่ไนโตร ไนเตรตสามารถทำได้หลายวิธี ไนเตรตของสารประกอบอะโรมาติกทำได้ง่าย ๆ โดยใช้ส่วนผสมของกรดไนตริกและกรดซัลฟิวริกเข้มข้น (อันแรกคือสารไนเตรตส่วนที่สองคือสารกำจัดน้ำ):
Trinitrotoluene เป็นที่รู้จักกันดีว่าเป็นวัตถุระเบิด ระเบิดจากการระเบิดเท่านั้น เผาไหม้ด้วยเปลวไฟควันโดยไม่มีการระเบิด
ไนเตรตของไฮโดรคาร์บอนอิ่มตัวดำเนินการโดยการบำบัดไฮโดรคาร์บอนด้วยกรดไนตริกเจือจางภายใต้ความร้อนและความดันสูง (ปฏิกิริยาของ M.I. Konovalov):
สารประกอบไนโตรมักถูกเตรียมโดยการทำปฏิกิริยาอัลคิลเฮไลด์กับซิลเวอร์ไนไตรท์:
เมื่อสารประกอบไนโตรลดลง จะเกิดเอมีนขึ้น
สารประกอบเฮเทอโรไซคลิกที่มีไนโตรเจน สารประกอบเฮเทอโรไซคลิกเป็นสารประกอบอินทรีย์ที่มีวงแหวน (รอบ) ในโมเลกุลของมันซึ่งในรูปแบบที่นอกเหนือจากอะตอมคาร์บอนแล้วอะตอมขององค์ประกอบอื่น ๆ ก็มีส่วนร่วมด้วย
เรียกว่าอะตอมของธาตุอื่นที่ประกอบเป็นเฮเทอโรไซเคิล เฮเทอโรอะตอม อย่างไรก็ตาม เฮเทอโรอะตอมที่พบมากที่สุดในเฮเทอโรไซเคิล ได้แก่ ไนโตรเจน ออกซิเจน และซัลเฟอร์ สารประกอบเฮเทอโรไซคลิกสามารถดำรงอยู่ได้กับธาตุหลากหลายชนิดที่มีวาเลนซีอย่างน้อยสองตัว
สารประกอบเฮเทอโรไซคลิกสามารถมีอะตอมในวงแหวนได้ตั้งแต่ 3, 4, 5, 6 อะตอมขึ้นไป อย่างไรก็ตาม มูลค่าสูงสุดมี เฮเทอโรไซเคิลห้าและหกสมาชิก. วัฏจักรเหล่านี้เช่นเดียวกับในชุดของสารประกอบคาร์โบไซคลิก จะก่อตัวได้ง่ายที่สุดและมีลักษณะพิเศษคือมีความแข็งแกร่งมากที่สุด เฮเทอโรไซเคิลอาจมีเฮเทอโรอะตอมหนึ่ง, สองอะตอมหรือมากกว่า
ในสารประกอบเฮเทอโรไซคลิกหลายชนิด โครงสร้างทางอิเล็กทรอนิกส์ของพันธะในวงแหวนจะเหมือนกับสารประกอบอะโรมาติก ดังนั้น สารประกอบเฮเทอโรไซคลิกทั่วไปจึงถูกกำหนดตามแบบแผนไม่เพียงแต่โดยสูตรที่มีพันธะคู่และพันธะเดี่ยวสลับกันเท่านั้น แต่ยังรวมถึงสูตรที่การควบคู่ของ p-อิเล็กตรอนถูกระบุด้วยวงกลมที่จารึกไว้ในสูตรด้วย
ชื่อเชิงประจักษ์มักจะใช้สำหรับเฮเทอโรไซเคิล
เฮเทอโรไซเคิลแบบห้าสมาชิก
เฮเทอโรไซเคิลแบบหกสมาชิก
สิ่งที่สำคัญอย่างยิ่งคือเฮเทอโรไซเคิลที่หลอมรวมกับวงแหวนเบนซีนหรือเฮเทอโรไซเคิลอื่น เช่น พิวรีน:
เฮเทอโรไซเคิลแบบหกสมาชิก ไพริดีน C5H5N - เฮเทอโรไซเคิลอะโรมาติกหกสมาชิกที่ง่ายที่สุดที่มีอะตอมไนโตรเจนหนึ่งอะตอม ถือได้ว่าเป็นอะนาล็อกของเบนซีนซึ่งกลุ่ม CH หนึ่งจะถูกแทนที่ด้วยอะตอมไนโตรเจน:
ไพริดีนเป็นของเหลวไม่มีสี เบากว่าน้ำเล็กน้อย มีกลิ่นไม่พึงประสงค์ ผสมกับน้ำในอัตราส่วนใดก็ได้ ไพริดีนและความคล้ายคลึงกันของมันถูกแยกออกจากน้ำมันถ่านหิน ในสภาพห้องปฏิบัติการไพริดีนสามารถสังเคราะห์ได้จากกรดไฮโดรไซยานิกและอะเซทิลีน:
คุณสมบัติทางเคมี ไพริดีนถูกกำหนดโดยการมีอยู่ของระบบอะโรมาติกที่ประกอบด้วย p-อิเล็กตรอนหกตัวและอะตอมไนโตรเจนที่มีคู่อิเล็กตรอนเดี่ยว
1. คุณสมบัติพื้นฐานไพริดีนเป็นเบสที่อ่อนกว่าอะลิฟาติกเอมีน สารละลายที่เป็นน้ำจะเปลี่ยนเป็นสีน้ำเงินลิตมัส:
เมื่อไพริดีนทำปฏิกิริยากับ กรดแก่เกลือไพริดิเนียมเกิดขึ้น:
2. คุณสมบัติอะโรมาติกไพริดีนทำปฏิกิริยาเช่นเดียวกับเบนซิน การทดแทนด้วยไฟฟ้าอย่างไรก็ตามกิจกรรมของมันในปฏิกิริยาเหล่านี้ต่ำกว่าของเบนซีนเนื่องจากมีอิเล็กโทรเนกาติวีตี้สูงของอะตอมไนโตรเจน ไพริดีนมีไนเตรตที่ 300 ° ด้วยเอาต์พุตต่ำ:
อะตอมไนโตรเจนในปฏิกิริยาการทดแทนอิเล็กโทรฟิลิกทำหน้าที่เป็นองค์ประกอบทดแทนชนิดที่ 2ดังนั้นการทดแทนอิเล็กโทรฟิลิกจึงเกิดขึ้น เมตา-ตำแหน่ง.
ต่างจากน้ำมันเบนซิน ไพริดีนสามารถทำปฏิกิริยาได้ การทดแทนนิวคลีโอฟิลิกเนื่องจากอะตอมไนโตรเจนดึงความหนาแน่นของอิเล็กตรอนจากระบบอะโรมาติกและ ortho-พารา-ตำแหน่งที่สัมพันธ์กับอะตอมไนโตรเจนจะหมดสิ้นไปด้วยอิเล็กตรอน ดังนั้นไพริดีนสามารถทำปฏิกิริยากับโซเดียมเอไมด์ทำให้เกิดเป็นส่วนผสมได้ ออร์โธ-และ คู่-อะมิโนไพริดีน (ปฏิกิริยาชิชิบาบิน):
ที่ การเติมไฮโดรเจนของไพริดีนระบบอะโรมาติกจะถูกทำลายและก่อตัวขึ้น พิเพอริดีน,ซึ่งเป็นเอมีนทุติยภูมิแบบไซคลิกและเป็นเบสที่แข็งแกร่งกว่าไพริดีนมาก:
ไพริมิดีน C4H4N2 - เฮเทอโรไซเคิลแบบหกสมาชิกที่มีอะตอมไนโตรเจนสองตัว ถือได้ว่าเป็นอะนาล็อกของเบนซีนซึ่งกลุ่ม CH สองกลุ่มจะถูกแทนที่ด้วยอะตอมไนโตรเจน:
เนื่องจากการมีอยู่ของอะตอมไนโตรเจนที่มีอิเล็กโทรเนกาติวิตี 2 อะตอมในวงแหวน ไพริมิดีนจึงออกฤทธิ์ในปฏิกิริยาการแทนที่อิเล็กโทรฟิลิกได้น้อยกว่าไพริดีนด้วยซ้ำคุณสมบัติพื้นฐานของมันยังเด่นชัดน้อยกว่าคุณสมบัติไพริดีนอีกด้วย
ความหมายหลักของไพริมิดีนคือเป็นบรรพบุรุษของกลุ่มเบสไพริมิดีน
ฐานไพริมิดีนเป็นอนุพันธ์ของไพริมิดีนซึ่งสารตกค้างซึ่งเป็นส่วนหนึ่งของกรดนิวคลีอิก: ยูราซิล, ไทมีน, ไซโตซีน
แต่ละฐานเหล่านี้มีอยู่ได้สองรูปแบบ ในสถานะอิสระ เบสจะอยู่ในรูปแบบอะโรมาติก และจะเข้าสู่องค์ประกอบของกรดนิวคลีอิกในรูปแบบ NH
สารประกอบที่มีวงแหวนห้าสมาชิก ไพโรล C4H4NH - เฮเทอโรไซเคิลแบบห้าสมาชิกที่มีอะตอมไนโตรเจนหนึ่งอะตอม
ระบบอะโรมาติกประกอบด้วย p-อิเล็กตรอน 6 ตัว (อย่างละ 1 ตัวจากอะตอมของคาร์บอน 4 ตัว และอิเล็กตรอน 1 คู่จากอะตอมไนโตรเจน) คู่อิเล็กตรอนของอะตอมไนโตรเจนในไพโรลต่างจากไพริดีนจึงเป็นส่วนหนึ่งของระบบอะโรมาติก ไพร์โรลแทบไม่มีคุณสมบัติพื้นฐานเลย
ไพโรลเป็นของเหลวไม่มีสี มีกลิ่นคล้ายคลอโรฟอร์ม ไพโรลละลายได้เล็กน้อยในน้ำ (< 6%), но растворим в органических растворителях. На воздухе быстро окисляется и темнеет.
ได้รับไพโรล การควบแน่นของอะเซทิลีนกับแอมโมเนีย:
หรือแอมโมไลซิสของวงแหวนห้าอะตอมกับเฮเทอโรอะตอมอื่น (ปฏิกิริยาของ Yuryev):
แข็งแกร่ง กรดแร่สามารถแยกอิเล็กตรอนคู่ของอะตอมไนโตรเจนออกจากระบบอะโรมาติกได้ ในขณะที่อะโรมาติกซิตี้ถูกรบกวน และไพโรลกลายเป็นสารประกอบที่ไม่เสถียรซึ่งจะเกิดปฏิกิริยาพอลิเมอร์ทันที เรียกว่าความไม่เสถียรของไพโรลในสภาพแวดล้อมที่เป็นกรด โรคกลัวกรด.
ไพโรลแสดงคุณสมบัติของกรดอ่อนมาก มันทำปฏิกิริยากับโพแทสเซียมเพื่อสร้างไพร์โรล-โพแทสเซียม:
ไพโรลเป็นสารประกอบอะโรมาติก มีแนวโน้มที่จะเกิดปฏิกิริยาทดแทนอิเล็กโทรฟิลิก ซึ่งเกิดขึ้นส่วนใหญ่ที่อะตอมเอคาร์บอน (ติดกับอะตอมไนโตรเจน)
การไฮโดรจิเนชันของไพร์โรลทำให้เกิดไพโรลิดีน ซึ่งเป็นเอมีนทุติยภูมิแบบไซคลิกซึ่งมีคุณสมบัติพื้นฐานดังต่อไปนี้:
ปูริน - เฮเทอโรไซเคิลซึ่งรวมถึงวงแหวนที่ประกบสองวง: ไพริดีนและอิมิดาโซล:
ระบบอะโรมาติกของพิวรีนประกอบด้วย p-อิเล็กตรอน 10 ตัว (อิเล็กตรอน 8 ตัวจากพันธะคู่ และอิเล็กตรอน 2 ตัวจากอะตอมไนโตรเจนแบบไพร์โรล) พิวรีนเป็นสารประกอบแอมโฟเทอริก คุณสมบัติพื้นฐานที่อ่อนแอของพิวรีนสัมพันธ์กับอะตอมไนโตรเจนของวงแหวนที่มีสมาชิก 6 ส่วน และคุณสมบัติที่เป็นกรดอ่อนนั้นสัมพันธ์กับหมู่ NH ของวงแหวนที่มีสมาชิก 5 สมาชิก
ความสำคัญหลักของพิวรีนก็คือเป็นบรรพบุรุษของกลุ่มเบสของพิวรีน
ฐานพิวรีนเป็นอนุพันธ์ของพิวรีนซึ่งสารตกค้างซึ่งเป็นส่วนหนึ่งของกรดนิวคลีอิก: อะดีนีน, กัวนีน
กรดนิวคลีอิก. กรดนิวคลีอิกเป็นสารประกอบโมเลกุลสูงตามธรรมชาติ (โพลีนิวคลีโอไทด์) ที่มีบทบาทอย่างมากในการจัดเก็บและการถ่ายทอดข้อมูลทางพันธุกรรมในสิ่งมีชีวิต น้ำหนักโมเลกุลของกรดนิวคลีอิกอาจแตกต่างกันตั้งแต่หลายแสนถึงหลายหมื่นล้าน พวกมันถูกค้นพบและแยกออกจากนิวเคลียสของเซลล์ในศตวรรษที่ 19 แต่ บทบาททางชีววิทยาได้รับการชี้แจงในช่วงครึ่งหลังของศตวรรษที่ 20 เท่านั้น
โครงสร้างของกรดนิวคลีอิกสามารถกำหนดได้โดยการวิเคราะห์ผลิตภัณฑ์จากการไฮโดรไลซิส การไฮโดรไลซิสของกรดนิวคลีอิกโดยสมบูรณ์ทำให้เกิดส่วนผสมของไพริมิดีนและเบสพิวรีน โมโนแซ็กคาไรด์ (บี-ไรโบสหรือบี-ดีออกซีไรโบส) และกรดฟอสฟอริก ซึ่งหมายความว่ากรดนิวคลีอิกถูกสร้างขึ้นจากเศษของสารเหล่านี้
เมื่อมีการไฮโดรไลซิสบางส่วนของกรดนิวคลีอิกจะเกิดส่วนผสมขึ้น นิวคลีโอไทด์,ซึ่งมีโมเลกุลที่ถูกสร้างขึ้นจากกรดฟอสฟอริกที่ตกค้าง โมโนแซ็กคาไรด์ (ไรโบสหรือดีออกซีไรโบส) และเบสไนโตรเจน (พิวรีนหรือไพริมิดีน) สารตกค้างของกรดฟอสฟอริกจะถูกจับกับอะตอมของคาร์บอนตัวที่ 3 หรือ 5 ของโมโนแซ็กคาไรด์ และสารตกค้างที่เป็นเบสจะถูกจับกับอะตอมของคาร์บอนตัวแรกของโมโนแซ็กคาไรด์ สูตรทั่วไปของนิวคลีโอไทด์:
โดยที่ X=OH สำหรับ ไรโบนิวคลีโอไทด์,สร้างขึ้นบนพื้นฐานของน้ำตาล และ X==H สำหรับ ดีออกซีไรโบนิวคลีโอไทด์,สร้างขึ้นบนพื้นฐานของดีออกซีไรโบส นิวคลีโอไทด์ของพิวรีนและไพริมิดีนขึ้นอยู่กับชนิดของฐานไนโตรเจน
นิวคลีโอไทด์เป็นหน่วยโครงสร้างหลักของกรดนิวคลีอิกซึ่งเป็นหน่วยโมโนเมอร์ กรดนิวคลีอิกที่ประกอบด้วยไรโบนิวคลีโอไทด์เรียกว่า กรดไรโบนิวคลีอิก (RNA)กรดนิวคลีอิกประกอบด้วยดีออกซีไรโบนิวคลีโอไทด์เรียกว่า กรดดีออกซีไรโบนิวคลีอิก (DNA)องค์ประกอบของโมเลกุล อาร์เอ็นเอรวมถึงนิวคลีโอไทด์ที่มีเบส อะดีนีน, กัวนีน, ไซโตซีนและยูราซิลองค์ประกอบของโมเลกุล ดีเอ็นเอรวมถึงนิวคลีโอไทด์ที่มี อะดีนีน, กวานีน, ไซโตซีน และไทมีนในการกำหนดฐานจะใช้ตัวย่อหนึ่งตัวอักษร: adenine - A, guanine - G, thymine - T, cytosine - C, uracil - U.
คุณสมบัติของ DNA และ RNA ถูกกำหนดโดยลำดับของเบสในสายพอลินิวคลีโอไทด์และโครงสร้างเชิงพื้นที่ของสายโซ่ ลำดับของเบสประกอบด้วยข้อมูลทางพันธุกรรม และโมโนแซ็กคาไรด์และกรดฟอสฟอริกที่ตกค้างมีบทบาททางโครงสร้าง (พาหะ เบส)
ในระหว่างการไฮโดรไลซิสบางส่วนของนิวคลีโอไทด์ สารตกค้างของกรดฟอสฟอริกจะถูกแยกออกและ นิวคลีโอไซด์,ซึ่งมีโมเลกุลประกอบด้วยพิวรีนหรือไพริมิดีนที่ตกค้างซึ่งเชื่อมโยงกับโมโนแซ็กคาไรด์ที่ตกค้าง - ไรโบสหรือดีออกซีไรโบส สูตรโครงสร้างพิวรีนหลักและนิวคลีโอไซด์ไพริมิดีน:
พิวรีนนิวคลีโอไซด์:
ไพริมิดีนนิวคลีโอไซด์:
ในโมเลกุล DNA และ RNA นิวคลีโอไทด์แต่ละตัวจะเชื่อมโยงกันเป็นสายโซ่โพลีเมอร์เดี่ยวเนื่องจากการก่อตัวของพันธะเอสเทอร์ระหว่างกรดฟอสฟอริกที่ตกค้างและหมู่ไฮดรอกซิลที่อะตอมของคาร์บอนที่ 3 และ 5 ของโมโนแซ็กคาไรด์:
โครงสร้างเชิงพื้นที่สายโซ่โพลีนิวคลีโอไทด์ของ DNA และ RNA ถูกกำหนดโดยการวิเคราะห์โครงสร้างเอ็กซ์เรย์ หนึ่งในการค้นพบทางชีวเคมีที่ใหญ่ที่สุดแห่งศตวรรษที่ 20 กลายเป็นแบบจำลองของโครงสร้าง DNA แบบเกลียวคู่ซึ่งเสนอในปี 1953 โดย J. Watson และ F. Crick ตามแบบจำลองนี้ โมเลกุล DNA นั้นเป็นเกลียวคู่และประกอบด้วยสายพอลินิวคลีโอไทด์สองสายที่บิดไปในทิศทางตรงกันข้ามรอบแกนร่วม ฐานของพิวรีนและไพริมิดีนอยู่ภายในเกลียว ส่วนฟอสเฟตและดีออกซีไรโบสตกค้างอยู่ด้านนอก เกลียวทั้งสองถูกยึดเข้าด้วยกันด้วยพันธะไฮโดรเจนระหว่างคู่เบส คุณสมบัติที่สำคัญที่สุดของ DNA คือการเลือกสรรในการสร้างพันธะ (การเสริม).ขนาดของฐานและเกลียวคู่ถูกเลือกโดยธรรมชาติในลักษณะที่ไทมีน (T) สร้างพันธะไฮโดรเจนกับอะดีนีน (A) เท่านั้น และไซโตซีน (C) กับกัวนีน (G) เท่านั้น
ดังนั้นเกลียวทั้งสองในโมเลกุล DNA จึงประกอบกัน ลำดับของนิวคลีโอไทด์ในเกลียวใดเกลียวหนึ่งเป็นตัวกำหนดลำดับของนิวคลีโอไทด์ในเกลียวอีกเกลียวหนึ่งโดยเฉพาะ
ในแต่ละคู่ของฐานที่เชื่อมต่อกันด้วยพันธะไฮโดรเจน หนึ่งในฐานคือพิวรีน และอีกฐานหนึ่งคือไพริมิดีน มันเป็นไปตามนั้น จำนวนทั้งหมดสารตกค้างเบสพิวรีนในโมเลกุล DNA เท่ากับจำนวนสารตกค้างเบสไพริมิดีน
ความยาวของสายโซ่พอลินิวคลีโอไทด์ DNA นั้นไม่จำกัดจริงๆ จำนวนคู่เบสในเกลียวคู่อาจแตกต่างกันตั้งแต่หลายพันคู่ในไวรัสที่ง่ายที่สุดไปจนถึงหลายร้อยล้านในมนุษย์
โมเลกุล RNA ต่างจาก DNA ตรงที่ประกอบด้วยสายพอลินิวคลีโอไทด์สายเดี่ยว จำนวนนิวคลีโอไทด์ในสายโซ่มีตั้งแต่ 75 ถึงหลายพัน และน้ำหนักโมเลกุลของ RNA สามารถแปรผันได้ตั้งแต่ 2,500 ถึงหลายล้าน สายพอลินิวคลีโอไทด์ของ RNA ไม่มีโครงสร้างที่กำหนดไว้อย่างเคร่งครัด
บทบาททางชีวภาพของกรดนิวคลีอิก DNA เป็นโมเลกุลหลักในสิ่งมีชีวิต เก็บข้อมูลทางพันธุกรรมที่ส่งต่อจากรุ่นหนึ่งไปยังอีกรุ่นหนึ่ง โมเลกุล DNA ประกอบด้วยองค์ประกอบของโปรตีนทั้งหมดในร่างกายในรูปแบบที่เข้ารหัส กรดอะมิโนแต่ละตัวที่ประกอบเป็นโปรตีนจะมีรหัสของตัวเองใน DNA ซึ่งก็คือลำดับเบสไนโตรเจน
DNA มีข้อมูลทางพันธุกรรมทั้งหมด แต่ไม่เกี่ยวข้องโดยตรงกับการสังเคราะห์โปรตีน RNA มีบทบาทเป็นตัวกลางระหว่าง DNA และบริเวณสังเคราะห์โปรตีนกระบวนการสังเคราะห์โปรตีนโดยใช้ข้อมูลทางพันธุกรรมสามารถแบ่งตามแผนผังออกเป็นสองขั้นตอนหลัก ได้แก่ การอ่านข้อมูล (การถอดเสียง)และการสังเคราะห์โปรตีน (ออกอากาศ).
เซลล์ประกอบด้วย RNA สามประเภทที่ทำหน้าที่ต่างกัน
1. ข้อมูลหรือเมทริกซ์ อาร์เอ็นเอ(ถูกกำหนดให้เป็น mRNA) อ่านและถ่ายโอนข้อมูลทางพันธุกรรมจาก DNA ที่มีอยู่ในโครโมโซมไปยังไรโบโซม โดยที่การสังเคราะห์โปรตีนเกิดขึ้นพร้อมกับลำดับกรดอะมิโนที่กำหนดไว้อย่างเคร่งครัด
2. ถ่ายโอนอาร์เอ็นเอ(tRNA) นำกรดอะมิโนไปยังไรโบโซม โดยเชื่อมต่อกันด้วยพันธะเปปไทด์ในลำดับเฉพาะ ซึ่งระบุโดย mRNA
3. ไรโบโซมอลอาร์เอ็นเอ (rRNA)เกี่ยวข้องโดยตรงกับการสังเคราะห์โปรตีนในไรโบโซม ไรโบโซมเป็นโครงสร้างโมเลกุลขนาดใหญ่ที่ซับซ้อนซึ่งประกอบด้วย rRNA สี่ตัวและโปรตีนหลายสิบชนิด. อันที่จริงไรโบโซมเป็นโรงงานโปรตีน
RNA ทุกประเภทถูกสังเคราะห์บนเกลียวคู่ของ DNA
ลำดับของเบสใน mRNA คือรหัสพันธุกรรมที่ควบคุมลำดับของกรดอะมิโนในโปรตีน มันถูกถอดรหัสในปี 1961-1966 ลักษณะเด่นของรหัสพันธุกรรมก็คือ มันเป็นสากลสำหรับสิ่งมีชีวิตทุกชนิดเบสเดียวกันใน RNA ต่างกัน (ไม่ว่าจะเป็น RNA ของมนุษย์หรือของไวรัส) จะสอดคล้องกับกรดอะมิโนชนิดเดียวกัน กรดอะมิโนแต่ละชนิดมีลำดับเบส 3 เบสของตัวเองเรียกว่า รหัสกรดอะมิโนบางชนิดถูกเข้ารหัสด้วยโคดอนหลายตัว ดังนั้น ลิวซีน ซีรีน และอาร์จินีนจึงสอดคล้องกับโคดอน 6 ตัว กรดอะมิโน 5 ตัว - โคดอน 4 ตัว ไอโซลิวซีน - โคดอน 3 ตัว กรดอะมิโน 9 ตัว - โคดอน 2 ตัว และเมไทโอนีนและทริปโตเฟน อย่างละ 1 ตัว โคดอน 3 ตัวเป็นสัญญาณให้หยุดการสังเคราะห์สายโซ่โพลีเปปไทด์ และเรียกว่าโคดอนเทอร์มิเนเตอร์
เอมีน เอมีนเป็นสารประกอบอินทรีย์ที่ถือได้ว่าเป็นอนุพันธ์ของแอมโมเนีย ซึ่งอะตอมไฮโดรเจน (หนึ่งอะตอมหรือมากกว่า) จะถูกแทนที่ด้วยอนุมูลไฮโดรคาร์บอน
เอมีนสามารถเป็นอะลิฟาติก (อิ่มตัวและไม่อิ่มตัว), อะลิไซคลิก, อะโรมาติก, เฮเทอโรไซคลิก ทั้งนี้ขึ้นอยู่กับลักษณะของอนุมูล พวกเขาแบ่งออกเป็น ประถมศึกษามัธยมศึกษาตอนปลายขึ้นอยู่กับจำนวนอะตอมของไฮโดรเจนที่ถูกแทนที่ด้วยอนุมูล
เกลือควอเทอร์นารีแอมโมเนียมชนิด + Cl- เป็นสารอะนาล็อกอินทรีย์ของเกลือแอมโมเนียมอนินทรีย์
ชื่อของเอมีนปฐมภูมิ มักจะได้มาจากชื่อของไฮโดรคาร์บอนที่เกี่ยวข้องโดยการเติมคำนำหน้า อะมิโน หรือสิ้นสุด -เอมีน . ชื่อของเอมีนทุติยภูมิและตติยภูมิ ส่วนใหญ่มักเกิดขึ้นตามหลักการของระบบการตั้งชื่อแบบเหตุผล โดยแสดงรายการอนุมูลที่มีอยู่ในสารประกอบ:
หลัก R—NH 2:CH 3—NH 2—เมทิลลามีน; C 6 H 5 -NH 2 - ฟีนิลามีน;
รอง R—NH—R": (CH 2)NH—ไดเมทิลเอมีน; C 6 H 5—NH—CH 3—เมทิลฟีนิลเอมีน;
ระดับอุดมศึกษา R—N(R")—R": (CH 3) 3 H—ไตรเมทิลลามีน; (C 6 H 5) 3 N - ไตรฟีนิลามีน
ใบเสร็จ. 1. ให้ความร้อนกับอัลคิลเฮไลด์ด้วยแอมโมเนียภายใต้ความดันจะนำไปสู่การอัลคิเลชันของแอมโมเนียตามลำดับซึ่งส่งผลให้เกิดการก่อตัวของส่วนผสมของเกลือของเอมีนปฐมภูมิทุติยภูมิและตติยภูมิซึ่งถูกดีไฮโดรฮาโลเจนภายใต้การกระทำของฐาน:
2. อะโรมาติกเอมีนได้จากการลดสารประกอบไนโตร:
สำหรับการลดลง คุณสามารถใช้สังกะสีหรือเหล็กในสภาพแวดล้อมที่เป็นกรด หรือใช้อลูมิเนียมในสภาพแวดล้อมที่เป็นด่าง
3. เอมีนต่ำได้จากการส่งส่วนผสมของแอลกอฮอล์และแอมโมเนียไปบนพื้นผิวของตัวเร่งปฏิกิริยา:
คุณสมบัติทางกายภาพอะลิฟาติกเอมีนที่ง่ายที่สุดที่ สภาวะปกติเป็นก๊าซหรือของเหลวที่มีจุดเดือดต่ำและมีกลิ่นฉุน เอมีนทั้งหมดเป็นสารประกอบเชิงขั้วซึ่งนำไปสู่การก่อตัวของพันธะไฮโดรเจนในเอมีนเหลว ดังนั้นจุดเดือดของพวกมันจึงเกินจุดเดือดของอัลเคนที่เกี่ยวข้อง ตัวแทนกลุ่มแรกของเอมีนจะละลายในน้ำ เมื่อโครงกระดูกคาร์บอนโตขึ้น ความสามารถในการละลายในน้ำจะลดลง เอมีนยังละลายได้ในตัวทำละลายอินทรีย์
คุณสมบัติทางเคมี. 1. คุณสมบัติพื้นฐานเนื่องจากอนุพันธ์ของแอมโมเนีย เอมีนทั้งหมดจึงมีคุณสมบัติพื้นฐาน โดยอะลิฟาติกเอมีนเป็นเบสที่แข็งแกร่งกว่าแอมโมเนีย และอะโรมาติกเอมีนเป็นเบสที่อ่อนกว่า นี่คือคำอธิบายโดยข้อเท็จจริงที่ว่าอนุมูล CH 3 -, C 2 H 5 — และการแสดงอื่นๆ อุปนัยเชิงบวก (+I)ส่งผลและเพิ่มความหนาแน่นของอิเล็กตรอนต่ออะตอมไนโตรเจน:
ส่งผลให้คุณสมบัติพื้นฐานเพิ่มขึ้น ในทางตรงกันข้าม อนุมูลฟีนิล C 6 H 5 จัดแสดง หน่วยความจำเชิงลบ (-M)ส่งผลและลดความหนาแน่นของอิเล็กตรอนต่ออะตอมไนโตรเจน:
ปฏิกิริยาอัลคาไลน์ของสารละลายเอมีนอธิบายได้โดยการก่อตัวของไฮดรอกซิลไอออนระหว่างปฏิกิริยาของเอมีนกับน้ำ:
เอมีนในรูปแบบบริสุทธิ์หรือในสารละลายทำปฏิกิริยากับกรดทำให้เกิดเกลือ:
โดยทั่วไปแล้วเกลือเอมีนจะเป็นของแข็งไม่มีกลิ่นซึ่งสามารถละลายน้ำได้สูง แม้ว่าเอมีนจะละลายได้ดีในตัวทำละลายอินทรีย์ แต่เกลือเอมีนละลายไม่ได้ เมื่ออัลคาลิสทำปฏิกิริยากับเกลือเอมีน เอมีนอิสระจะถูกปล่อยออกมา:
2. การเผาไหม้เอมีนเผาไหม้ในออกซิเจนเพื่อสร้างไนโตรเจน คาร์บอนไดออกไซด์และน้ำ:
3. ปฏิกิริยากับกรดไนตรัส ก) อะลิฟาติกเอมีนปฐมภูมิ ภายใต้อิทธิพลของกรดไนตรัส เปลี่ยนเป็นแอลกอฮอล์:
ข) เอมีนอะโรมาติกปฐมภูมิ ภายใต้อิทธิพลของ HNO 2 เปลี่ยนเป็นเกลือไดโซเนียม:
c) เอมีนทุติยภูมิ (อะลิฟาติกและอะโรมาติก) ให้สารประกอบไนโตรโซ - สารที่มีกลิ่นเฉพาะตัว:
ตัวแทนที่สำคัญที่สุดของเอมีนอะลิฟาติกเอมีนที่ง่ายที่สุดคือ เมทิลลามีน, ไดเมทิลลามีน, ไดเอทิลเอมีน — ใช้ในการสังเคราะห์สารยาและผลิตภัณฑ์อื่น ๆ ของการสังเคราะห์สารอินทรีย์ เฮกซาเมทิลีนไดเอมีน NH 2 -(CH 2) 2 -NH 6 เป็นหนึ่งในวัตถุดิบเริ่มต้นในการได้รับความสำคัญ วัสดุโพลีเมอร์ไนลอน.
สวรรค์ C 6 H 5 NH 2 - ที่สำคัญที่สุดคือเอมีนอะโรมาติก เป็นของเหลวมันไม่มีสี ละลายน้ำได้เล็กน้อย สำหรับการตรวจหาสวรรค์ในเชิงคุณภาพ ใช้ปฏิกิริยากับน้ำโบรมีนซึ่งส่งผลให้เกิดการตกตะกอนสีขาวของ 2,4,6-tribromoaniline:
สวรรค์ใช้ในการผลิตสีย้อม ยา, พลาสติก ฯลฯ
กรดอะมิโน. กรดอะมิโนเป็นสารประกอบอินทรีย์สองฟังก์ชันที่ประกอบด้วยหมู่คาร์บอกซิล -COOH และหมู่อะมิโน -NH 2 . ขึ้นอยู่กับ ตำแหน่งสัมพัทธ์ทั้งสองกลุ่มการทำงานมีความโดดเด่นด้วยกรดอะมิโน a -, b -, g - ฯลฯ:
ตัวอักษรกรีกที่อะตอมของคาร์บอนบ่งบอกถึงระยะห่างจากหมู่คาร์บอกซิล โดยปกติแล้วจะมีเพียงก -กรดอะมิโน,เพราะกรดอะมิโนชนิดอื่นๆ ไม่พบในธรรมชาติ
โปรตีนประกอบด้วยกรดอะมิโนพื้นฐาน 20 ชนิด (ดูตาราง)
กรดอะมิโนที่สำคัญที่สุดตามสูตรทั่วไป
|
ชื่อ |
—ร |
|
ไกลซีน |
—น |
|
อลานิน |
—ช 3 |
|
ซีสเตอีน |
—ช 2 —ช |
|
เซริน |
—ช 2 —โอ้ |
|
ฟีนิลอะลานีน |
—ช 2 —ค 6 ชม 5 |
|
ไทโรซีน |
|
|
กรดกลูตามิก |
-CH 2 -CH 2 -COOH |
|
ไลซีน |
—(CH 2) 4 —NH 2 |
กรดอะมิโนธรรมชาติทั้งหมดสามารถแบ่งออกเป็นกลุ่มหลักได้ดังต่อไปนี้:
1) กรดอะมิโนอิ่มตัวอะลิฟาติก(ไกลซีน, อะลานีน);
2) กรดอะมิโนที่มีกำมะถัน(ซิสเทอีน);
3) กรดอะมิโนที่มีหมู่อะลิฟาติกไฮดรอกซิล(ซีรีน);
4) กรดอะมิโนอะโรมาติก(ฟีนิลอะลานีน, ไทโรซีน);
5) กรดอะมิโนที่มีอนุมูลกรด(กรดกลูตามิก);
6) กรดอะมิโนที่มีอนุมูลพื้นฐาน(ไลซีน).
ไอโซเมอริซึม.ในกรดอะมิโนทั้งหมด ยกเว้นไกลซีน อะตอมของอะ-คาร์บอนจะเชื่อมต่อกับองค์ประกอบทดแทนที่แตกต่างกัน 4 ชนิด ดังนั้นกรดอะมิโนทั้งหมดนี้จึงสามารถดำรงอยู่ได้ในรูปของไอโซเมอร์ 2 ตัว ซึ่งเป็นภาพสะท้อนของกันและกัน
ใบเสร็จ. 1. ไฮโดรไลซิสของโปรตีนมักจะสร้างส่วนผสมที่ซับซ้อนของกรดอะมิโน อย่างไรก็ตาม มีการพัฒนาวิธีการจำนวนหนึ่งที่ทำให้สามารถรับกรดอะมิโนบริสุทธิ์จากส่วนผสมที่ซับซ้อนได้
2. การทดแทนฮาโลเจนด้วยหมู่อะมิโนในกรดฮาโลเจนที่สอดคล้องกัน วิธีการรับกรดอะมิโนนี้คล้ายคลึงกับการได้รับเอมีนจากอนุพันธ์ของฮาโลเจนของอัลเคนและแอมโมเนียอย่างสมบูรณ์:
คุณสมบัติทางกายภาพกรดอะมิโนเป็นสารผลึกแข็ง ละลายได้สูงในน้ำ และละลายได้เล็กน้อยในตัวทำละลายอินทรีย์ มีกรดอะมิโนหลายชนิด รสหวาน. พวกเขาละลายที่ อุณหภูมิสูงและมักจะสลายตัวไปตามกระบวนการ พวกเขาไม่สามารถเข้าสู่สถานะเป็นไอได้
คุณสมบัติทางเคมี. กรดอะมิโนเป็นสารประกอบแอมโฟเทริกอินทรีย์ประกอบด้วยหมู่ฟังก์ชัน 2 หมู่ที่มีลักษณะตรงกันข้ามกันในโมเลกุล ได้แก่ หมู่อะมิโนที่มีคุณสมบัติพื้นฐาน และหมู่คาร์บอกซิลที่มีคุณสมบัติเป็นกรด กรดอะมิโนทำปฏิกิริยากับทั้งกรดและเบส:
เมื่อกรดอะมิโนละลายในน้ำ หมู่คาร์บอกซิลจะกำจัดไฮโดรเจนไอออน ซึ่งสามารถเกาะติดกับหมู่อะมิโนได้ สิ่งนี้สร้าง เกลือภายในโมเลกุลที่เป็นไอออนสองขั้ว:
การเปลี่ยนแปลงของกรด-เบสของกรดอะมิโนในสภาพแวดล้อมต่างๆ สามารถแสดงได้ด้วยแผนภาพต่อไปนี้:
สารละลายที่เป็นน้ำของกรดอะมิโนมีสภาพแวดล้อมที่เป็นกลาง เป็นด่างหรือเป็นกรด ขึ้นอยู่กับจำนวนหมู่ฟังก์ชัน ดังนั้นกรดกลูตามิกจึงก่อให้เกิดสารละลายที่เป็นกรด (สองกลุ่ม -COOH, หนึ่ง -NH 2), ไลซีน - อัลคาไลน์ (หนึ่งกลุ่ม -COOH, สอง -NH 2)
กรดอะมิโนสามารถทำปฏิกิริยากับแอลกอฮอล์เมื่อมีก๊าซไฮโดรเจนคลอไรด์เกิดเป็นเอสเทอร์:
คุณสมบัติที่สำคัญที่สุดของกรดอะมิโนคือความสามารถในการควบแน่นเพื่อสร้างเปปไทด์
เปปไทด์ เปปไทด์ เป็นผลิตภัณฑ์ควบแน่นของโมเลกุลกรดอะมิโนตั้งแต่ 2 โมเลกุลขึ้นไป โมเลกุลของกรดอะมิโนสองตัวสามารถทำปฏิกิริยากันเพื่อกำจัดโมเลกุลของน้ำและสร้างผลิตภัณฑ์ที่มีชิ้นส่วนเชื่อมโยงกัน พันธะเปปไทด์—СО—NH —.
สารประกอบที่เกิดขึ้นเรียกว่าไดเปปไทด์ โมเลกุลไดเปปไทด์ เช่น กรดอะมิโน ประกอบด้วยหมู่อะมิโนและหมู่คาร์บอกซิล และสามารถทำปฏิกิริยากับโมเลกุลของกรดอะมิโนได้อีก 1 โมเลกุล:
ผลิตภัณฑ์ปฏิกิริยาเรียกว่าไตรเปปไทด์ กระบวนการเพิ่มสายโซ่เปปไทด์สามารถดำเนินต่อไปได้ในหลักการอย่างไม่มีกำหนด (การควบแน่นหลายตัว) และนำไปสู่สารที่มีน้ำหนักโมเลกุลสูงมาก (โปรตีน)
คุณสมบัติหลักของเปปไทด์คือความสามารถในการไฮโดรไลซ์ในระหว่างการไฮโดรไลซิส จะเกิดการแตกแยกของสายเปปไทด์ทั้งหมดหรือบางส่วน และเปปไทด์ที่สั้นกว่าซึ่งมีน้ำหนักโมเลกุลต่ำกว่าหรือกรด α-อะมิโนที่ประกอบเป็นสายโซ่จะถูกสร้างขึ้น การวิเคราะห์ผลิตภัณฑ์จากการไฮโดรไลซิสโดยสมบูรณ์ช่วยให้เราสามารถระบุองค์ประกอบของกรดอะมิโนของเปปไทด์ได้ การไฮโดรไลซิสโดยสมบูรณ์เกิดขึ้นเมื่อเปปไทด์ถูกให้ความร้อนเป็นเวลานานด้วยกรดไฮโดรคลอริกเข้มข้น
การไฮโดรไลซิสของเปปไทด์สามารถเกิดขึ้นได้ในสภาพแวดล้อมที่เป็นกรดหรือด่างรวมทั้งภายใต้การทำงานของเอนไซม์ เกลือของกรดอะมิโนเกิดขึ้นในสภาพแวดล้อมที่เป็นกรดและเป็นด่าง:
การไฮโดรไลซิสของเอนไซม์มีความสำคัญเนื่องจากเกิดขึ้น เลือกสรรต . e. อนุญาตให้มีการแตกแยกของส่วนที่กำหนดไว้อย่างเคร่งครัดของสายเปปไทด์
ปฏิกิริยาเชิงคุณภาพต่อกรดอะมิโน 1) กรดอะมิโนทั้งหมดถูกออกซิไดซ์ นินไฮดรินด้วยการก่อตัวของผลิตภัณฑ์ที่มีสีเข้า สีฟ้าม่วง. ปฏิกิริยานี้สามารถใช้เพื่อวัดปริมาณกรดอะมิโนโดยสเปกโตรโฟโตเมทรี 2) เมื่อกรดอะมิโนอะโรมาติกถูกให้ความร้อนด้วยกรดไนตริกเข้มข้น จะเกิดไนเตรชันของวงแหวนเบนซีนและสารประกอบมีสี สีเหลือง. ปฏิกิริยานี้เรียกว่า แซนโทโปรตีน(จากภาษากรีก แซนโทส -สีเหลือง).
กระรอก โปรตีนเป็นโพลีเปปไทด์จากธรรมชาติด้วย ค่าสูงน้ำหนักโมเลกุล (ตั้งแต่ 10,000 ถึงหลักสิบล้าน) พวกมันเป็นส่วนหนึ่งของสิ่งมีชีวิตทุกชนิดและทำหน้าที่ทางชีววิทยาที่หลากหลาย
โครงสร้าง.สามารถแบ่งระดับได้สี่ระดับในโครงสร้างของสายโซ่โพลีเปปไทด์ โครงสร้างปฐมภูมิของโปรตีนคือลำดับเฉพาะของกรดอะมิโนในสายโซ่โพลีเปปไทด์ สายเปปไทด์มีโครงสร้างเชิงเส้นในโปรตีนจำนวนเล็กน้อยเท่านั้น ในโปรตีนส่วนใหญ่ สายโซ่เปปไทด์จะพับในลักษณะใดลักษณะหนึ่งในอวกาศ
โครงสร้างรองคือโครงสร้างของสายโซ่โพลีเปปไทด์ กล่าวคือ การบิดสายโซ่ในอวกาศเนื่องจากพันธะไฮโดรเจนระหว่างหมู่ NH และ CO วิธีการหลักในการวางโซ่คือเกลียว
โครงสร้างระดับตติยภูมิของโปรตีนคือโครงสร้างสามมิติของเกลียวบิดในอวกาศ โครงสร้างตติยภูมิเกิดขึ้นเนื่องจากสะพานไดซัลไฟด์ -S-S- ระหว่างซีสเตอีนที่ตกค้างอยู่ในตำแหน่งต่าง ๆ ของสายโซ่โพลีเปปไทด์ มีส่วนร่วมในการก่อตัวของโครงสร้างระดับอุดมศึกษาด้วย ปฏิกิริยาอิออนกลุ่มที่มีประจุตรงข้าม NH 3 + และ COO- และ ปฏิกิริยาที่ไม่ชอบน้ำกล่าวคือแนวโน้มของโมเลกุลโปรตีนที่จะพับเพื่อให้สารไฮโดรคาร์บอนที่ไม่ชอบน้ำอยู่ภายในโครงสร้าง
โครงสร้างระดับตติยภูมิเป็นรูปแบบการจัดโปรตีนเชิงพื้นที่สูงสุดอย่างไรก็ตาม มีโปรตีนบางชนิด (เช่น เฮโมโกลบิน) โครงสร้างควอเทอร์นารีซึ่งเกิดขึ้นเนื่องจากปฏิสัมพันธ์ระหว่างสายโพลีเปปไทด์ที่แตกต่างกัน
คุณสมบัติทางกายภาพโปรตีนมีความหลากหลายมากและถูกกำหนดโดยโครงสร้างของมัน โดย คุณสมบัติทางกายภาพโปรตีนแบ่งออกเป็น 2 ประเภท: โปรตีนทรงกลมละลายในน้ำหรือเกิดเป็นสารละลายคอลลอยด์ โปรตีนไฟบริลลาร์ไม่ละลายในน้ำ
คุณสมบัติทางเคมี. 1 . การทำลายโครงสร้างทุติยภูมิและตติยภูมิของโปรตีนในขณะที่ยังคงรักษาโครงสร้างปฐมภูมิไว้เรียกว่าการสูญเสียสภาพธรรมชาติ . มันเกิดขึ้นเมื่อถูกความร้อน การเปลี่ยนแปลงความเป็นกรดของสิ่งแวดล้อม หรือการสัมผัสกับรังสี ตัวอย่างของการสูญเสียสภาพธรรมชาติคือการแข็งตัวของไข่ขาวเมื่อไข่ต้ม การเสียสภาพสามารถย้อนกลับหรือกลับไม่ได้การสูญเสียสภาพธรรมชาติที่ไม่สามารถกลับคืนสภาพเดิมได้อาจเกิดจากการก่อตัวของสารที่ไม่ละลายน้ำเมื่อโปรตีนสัมผัสกับเกลือของโลหะหนัก - ตะกั่วหรือปรอท
2. การไฮโดรไลซิสของโปรตีนคือการทำลายโครงสร้างหลักในสารละลายที่เป็นกรดหรือด่างโดยไม่สามารถกลับคืนสภาพเดิมได้ด้วยการก่อตัวของกรดอะมิโน ด้วยการวิเคราะห์ผลิตภัณฑ์ไฮโดรไลซิส ทำให้สามารถระบุองค์ประกอบเชิงปริมาณของโปรตีนได้
3. สำหรับโปรตีนนั้น มีหลายสิ่งที่รู้กัน ปฏิกิริยาเชิงคุณภาพ สารประกอบทั้งหมดที่มีพันธะเปปไทด์จะให้สีม่วงเมื่อสัมผัสกับเกลือของคอปเปอร์ (II) ในสารละลายอัลคาไลน์ ปฏิกิริยานี้เรียกว่า ไบยูเรตโปรตีนที่มีกรดอะมิโนอะโรมาติกตกค้าง (ฟีนิลอะลานีน, ไทโรซีน) จะให้สีเหลืองเมื่อสัมผัสกับความเข้มข้น กรดไนตริก (แซนโทโปรตีนปฏิกิริยา).
ความสำคัญทางชีวภาพของโปรตีน:
1. ทุกอย่าง ปฏิกริยาเคมีเกิดขึ้นในร่างกายเมื่อมีตัวเร่งปฏิกิริยา - เอนไซม์เอนไซม์ที่รู้จักทั้งหมดคือโมเลกุลโปรตีน โปรตีนเป็นตัวเร่งปฏิกิริยาที่ทรงพลังและคัดเลือกได้ดีมาก พวกมันเร่งปฏิกิริยาหลายล้านครั้ง และแต่ละปฏิกิริยาก็มีเอนไซม์ตัวเดียว
2. โปรตีนบางชนิดทำหน้าที่ขนส่งและขนส่งโมเลกุลหรือไอออนไปยังบริเวณที่มีการสังเคราะห์หรือการสะสม เช่น โปรตีนที่มีอยู่ในเลือด เฮโมโกลบินนำออกซิเจนไปยังเนื้อเยื่อและโปรตีน ไมโอโกลบินเก็บออกซิเจนไว้ในกล้ามเนื้อ
3. โปรตีนนั้น วัสดุก่อสร้างเซลล์. เนื้อเยื่อพยุงกล้ามเนื้อและผิวหนังถูกสร้างขึ้นจากเนื้อเยื่อเหล่านี้
4. โปรตีนมีบทบาทสำคัญใน ระบบภูมิคุ้มกันร่างกาย. มีโปรตีนจำเพาะ (แอนติบอดี)ซึ่งสามารถจดจำและจับกับวัตถุแปลกปลอม เช่น ไวรัส แบคทีเรีย เซลล์แปลกปลอม
5. โปรตีนของตัวรับรับรู้และส่งสัญญาณที่มาจากเซลล์ข้างเคียงหรือจาก สิ่งแวดล้อม. ตัวอย่างเช่น ผลกระทบของแสงบนเรตินาของดวงตาจะถูกรับรู้โดยโรดอปซินรับแสง ตัวรับที่ถูกกระตุ้นโดยสารที่มีน้ำหนักโมเลกุลต่ำ เช่น อะเซทิลโคลีน จะส่งกระแสประสาทที่จุดเชื่อมต่อของเซลล์ประสาท
จากรายการหน้าที่ของโปรตีนข้างต้น แสดงให้เห็นชัดเจนว่าโปรตีนมีความสำคัญต่อสิ่งมีชีวิตใดๆ และเป็นส่วนประกอบที่สำคัญที่สุดของอาหาร ในระหว่างกระบวนการย่อยอาหาร โปรตีนจะถูกไฮโดรไลซ์เป็นกรดอะมิโน ซึ่งทำหน้าที่เป็นวัสดุเริ่มต้นสำหรับการสังเคราะห์โปรตีนที่จำเป็นสำหรับสิ่งมีชีวิตที่กำหนด มีกรดอะมิโนหลายชนิดที่ร่างกายไม่สามารถสังเคราะห์เองได้และได้มาจากอาหารเท่านั้นกรดอะมิโนเหล่านี้เรียกว่า ไม่สามารถถูกแทนที่ได้
บรรยาย:คุณสมบัติทางเคมีเฉพาะของสารประกอบอินทรีย์ที่มีไนโตรเจน: เอมีนและกรดอะมิโน
เอมีน คุณสมบัติของโครงสร้าง
คุณรู้อยู่แล้วว่าโมเลกุลของสารประกอบอินทรีย์ประกอบด้วยอะตอมของคาร์บอน ไฮโดรเจน และออกซิเจน แต่ในหมู่พวกเขามีอะตอมไนโตรเจนด้วย เป็นสารประกอบอินทรีย์ที่มีไนโตรเจน เช่น กรดอะมิโน โปรตีน และกรดนิวคลีอิก ซึ่งเป็นพื้นฐานของสิ่งมีชีวิตบนโลก สารประกอบที่มีไนโตรเจนที่ง่ายที่สุดคือเอมีน
เอมีน– เหล่านี้เป็นสารประกอบอินทรีย์ที่เป็นอนุพันธ์ของแอมโมเนียในโมเลกุลที่อะตอมไฮโดรเจนหนึ่งอะตอมหรือมากกว่านั้นถูกแทนที่ด้วยอนุมูลไฮโดรคาร์บอน (R)
ตามคำกล่าวนี้กล่าวคือ ขึ้นอยู่กับจำนวนหมู่อะมิโนของ NH2 เอมีนจะถูกแบ่งออกเป็น:
หลัก,
รองและ
ระดับอุดมศึกษา

อะตอมไนโตรเจนในโมเลกุลเอมีนพร้อมเสมอที่จะให้อิเล็กตรอนคู่เดียวของมันแก่อีกอะตอมหนึ่ง ดังนั้นจึงเป็นผู้บริจาค ดังนั้นการเชื่อมต่อของไฮโดรเจนไอออนบวกกับอะตอมไนโตรเจนในโมเลกุลเอมีนจึงเกิดขึ้นโดยใช้กลไกของผู้บริจาคและตัวรับ ด้วยเหตุนี้ เอมีน เช่น แอมโมเนีย จึงมีคุณสมบัติพื้นฐานที่เด่นชัดพอสมควร
เอมีนแบ่งออกเป็น: ขึ้นอยู่กับชนิดของอนุมูลที่เกี่ยวข้องกับอะตอมไนโตรเจน
อะลิฟาติก (CH 3 -N<) и
อะโรมาติก (C 6 H 5 -N<).
ไอโซเมอริซึมของอะลิฟาติกเอมีน:

อะลิฟาติกเอมีนหรือที่เรียกว่าเอมีนอิ่มตัวนั้นเป็นเบสที่แข็งแกร่งกว่าแอมโมเนีย นี่เป็นเพราะความจริงที่ว่าสารทดแทนไฮโดรคาร์บอนในเอมีนมีผลอุปนัยเชิงบวก (+I) ด้วยเหตุนี้ความหนาแน่นของอิเล็กตรอนในอะตอมไนโตรเจนจึงเพิ่มขึ้น กระบวนการนี้อำนวยความสะดวกอย่างมากในการโต้ตอบกับไอออนบวก H +
ไอโซเมอร์ของอะโรมาติกเอมีน:

อะโรมาติกเอมีนมีคุณสมบัติพื้นฐานที่อ่อนแอกว่าเมื่อเปรียบเทียบกับแอมโมเนีย สิ่งนี้อธิบายได้จากข้อเท็จจริงที่ว่าคู่อิเล็กตรอนเดี่ยวของอะตอมไนโตรเจนเลื่อนไปทางระบบอะโรมาติก π ของวงแหวนเบนซีน ต่อจากนั้นความหนาแน่นของอิเล็กตรอนในอะตอมไนโตรเจนจะค่อยๆลดลง
คุณสมบัติทางเคมีของเอมีน
การมีอยู่ของคู่อิเล็กตรอนบนอะตอมไนโตรเจนทำให้มีคุณสมบัติพื้นฐานของเอมีน เอมีนอิ่มตัวปฐมภูมิเนื่องจากคุณสมบัติพื้นฐานที่แข็งแกร่งกว่า จึงทำปฏิกิริยากับน้ำได้ดีกว่าแอมโมเนียเล็กน้อย ในทางกลับกัน ความเป็นพื้นฐานของเอมีนอิ่มตัวทุติยภูมิจะมากกว่าเอมีนปฐมภูมิ การแสดงคุณสมบัติพื้นฐานโดยเอมีนระดับตติยภูมินั้นไม่ชัดเจนนักเนื่องจากอะตอมไนโตรเจนในพวกมันมักจะถูกป้องกันโดยอนุมูลไฮโดรคาร์บอนซึ่งรบกวนการแสดงคุณสมบัติพื้นฐานของมัน
เอมีนทำปฏิกิริยาย้อนกลับกับน้ำได้ สารละลายเอมีนที่เป็นน้ำเป็นตัวกลางที่เป็นด่างซึ่งเป็นผลมาจากการแยกตัวของฐานที่เกิดขึ้น ปฏิกิริยาทั่วไปมีลักษณะดังนี้:
RNH 2 + H 2 O<->RNH 3 + + โอ้ -
เอมีนอิ่มตัวอิสระและสารละลายที่เป็นน้ำจะทำปฏิกิริยากับกรดเพื่อสร้างเกลือ เช่น:
CH 3 NH 2 + H 2 SO 4 → HSO 4
C 6 H 5 NH 2 + HCl → Cl
เกลือเอมีนเป็นแบบอะนาล็อกของเกลือแอมโมเนียมและเป็นของแข็ง ละลายได้ดีในน้ำและละลายได้ไม่ดีในตัวทำละลายอินทรีย์ที่ไม่มีขั้ว ในการทำปฏิกิริยากับด่างเมื่อถูกความร้อน เอมีนอิสระจะถูกปล่อยออกมาจากเกลือเอมีน:
[ช 3 NH 3 ] แคล+ NaOH → CH3NH2+ นา แคล+ น้ำ
เอมีนอิ่มตัวปฐมภูมิทำปฏิกิริยากับกรดไนตรัสเพื่อสร้างแอลกอฮอล์ ก๊าซไนโตรเจน N2 และน้ำ:
RNH 2 + HNO 2 → ROH + N 2 + H 2 O
นี่เป็นปฏิกิริยาเชิงคุณภาพของเอมีนอิ่มตัวปฐมภูมิและใช้เพื่อแยกความแตกต่างจากเอมีนทุติยภูมิและตติยภูมิ
เอมีนทุติยภูมิในปฏิกิริยาเดียวกันจะเกิดเป็นของเหลวมันที่มีกลิ่น - N-nitrosamines:
R 2 NH + H O- ยังไม่มีข้อความ=O → ร 2 ยังไม่มีข้อความ=O+น้ำ2O
เอมีนระดับอุดมศึกษาไม่ทำปฏิกิริยากับกรดไนตรัส
- เอมีนได้รับปฏิกิริยาทดแทนนิวคลีโอฟิลิก:
CH 3 CH 2 ห้องนอน + ช 3 ช.2 เอ็นเอช 2 → (ช 3 ช.2 ) 2 NH2+ บ- ช.2 ช 3
- ปฏิกิริยาระหว่างเอมีนปฐมภูมิและทุติยภูมิกับกรดคาร์บอกซิลิกทำให้เกิดอะซิเลชันซึ่งส่งผลให้เกิดสารประกอบอินทรีย์ที่สำคัญที่สุด - เอไมด์:

การเผาไหม้เอมีนโดยสมบูรณ์ทำให้เกิดคาร์บอนไดออกไซด์ น้ำ และไนโตรเจน:
4C nH 2n+3 N + (6n+3)O 2 → 4nCO 2 + (4n+6)H 2 O
 ให้เราพิจารณาคุณสมบัติทางเคมีของอะนิลีน (อะมิโนเบนซีน) ซึ่งเป็นอะโรมาติกเอมีนที่ง่ายที่สุด หมู่อะมิโนในโมเลกุลของสารนี้เชื่อมต่อโดยตรงกับวงแหวนอะโรมาติก คุณสมบัติพื้นฐานของสวรรค์นั้นอ่อนกว่าอะลิฟาติกเอมีนมาก ดังนั้นจึงไม่เกิดปฏิกิริยาของสวรรค์กับน้ำและกรดอ่อน (เช่น กรดคาร์บอนิก)
ให้เราพิจารณาคุณสมบัติทางเคมีของอะนิลีน (อะมิโนเบนซีน) ซึ่งเป็นอะโรมาติกเอมีนที่ง่ายที่สุด หมู่อะมิโนในโมเลกุลของสารนี้เชื่อมต่อโดยตรงกับวงแหวนอะโรมาติก คุณสมบัติพื้นฐานของสวรรค์นั้นอ่อนกว่าอะลิฟาติกเอมีนมาก ดังนั้นจึงไม่เกิดปฏิกิริยาของสวรรค์กับน้ำและกรดอ่อน (เช่น กรดคาร์บอนิก)
สวรรค์ทำปฏิกิริยากับกรดอนินทรีย์ที่แรงและปานกลางเพื่อสร้างฟีนิลแอมโมเนียม เช่น:
ค 6 ชั่วโมง 5 NH 2 + HCl → C 6 H 5 N H 3 Cล
เกลือฟีนิลแอมโมเนียม C 6 H 5 NH 3 + ละลายได้สูงในน้ำ แต่ไม่ละลายในตัวทำละลายอินทรีย์ที่ไม่มีขั้ว
กลุ่มอะมิโนของอะโรมาติกเอมีน โดยเฉพาะอย่างยิ่งอะนิลีน ถูกดึงเข้าไปในวงแหวนอะโรมาติกจะช่วยลดความหนาแน่นของอิเล็กตรอนบนอะตอมไนโตรเจน แต่จะเพิ่มขึ้นในวงแหวนอะโรมาติก ดังนั้นปฏิกิริยาการแทนที่ด้วยอิเล็กโทรฟิลิก (ที่มีฮาโลเจน) ดำเนินไปได้ง่ายขึ้นมาก โดยเฉพาะในตำแหน่งออร์โธและพารา ตัวอย่างเช่น อะนิลีนทำปฏิกิริยากับน้ำโบรมีนได้ง่าย ทำให้เกิดตะกอนสีขาวเป็น 2,4,6-ไตรโบรโมอะนิลีน:

นี่เป็นปฏิกิริยาเชิงคุณภาพต่อสวรรค์
อะนิลีนทำปฏิกิริยากับกรดไนตรัสที่ 0 0 C เกลือไดอาโซเนียมจะเกิดขึ้นซึ่งมีความสำคัญในทางปฏิบัติอย่างยิ่งและใช้ในการสังเคราะห์สีย้อมเอโซและสารประกอบอื่น ๆ:
C 6 H 5 NH 2 + KNO 2 + 2HCl → + Cl - + KCl + 2H 2 O
ผลิตภัณฑ์ของปฏิกิริยานี้คือฟีนิลไดอาโซเนียมคลอไรด์, โพแทสเซียมคลอไรด์และน้ำ
เมื่อปฏิกิริยาประเภทนี้เกิดขึ้นที่อุณหภูมิสูง ไนโตรเจนจะถูกปล่อยออกมา และอะนิลีนจะถูกแปลงเป็นฟีนอล:
C 6 H 5 NH 2 + นาโน 2 + H 2 SO 4 → C 6 H 5 -OH + N2+นา สสส.4 + น้ำ
อัลคิเลชั่นของอะนิลีนกับไฮโดรคาร์บอนที่มีฮาโลเจนจะก่อให้เกิดเอมีนทุติยภูมิและตติยภูมิ
คุณสมบัติทางเคมีของกรดอะมิโน
กรดอะมิโน- สารประกอบอินทรีย์ที่มีโมเลกุลมีสองหมู่ฟังก์ชัน - อะมิโน (-NH 2) และคาร์บอกซี- (-COOH)
สูตรกรดอะมิโนทั่วไป: (NH2)xR(COOH)y,โดยที่ x และ y มักเป็น 1 หรือ 2
 การมีอยู่ของหมู่อะมิโนและคาร์บอกซีในโมเลกุลของสารประกอบเหล่านี้อธิบายคุณสมบัติทางเคมีของกรดอะมิโน ซึ่งคล้ายกับเอมีนและกรดคาร์บอกซิลิก ดังนั้นกรดอะมิโนจึงแสดงคุณสมบัติพื้นฐานของสารประกอบที่มีหมู่อะมิโนและคุณสมบัติที่เป็นกรดซึ่งเป็นลักษณะของสารประกอบที่มีหมู่คาร์บอกซิล ดังนั้นกรดอะมิโนจึงเป็นสารประกอบอินทรีย์แบบแอมโฟเทอริก
การมีอยู่ของหมู่อะมิโนและคาร์บอกซีในโมเลกุลของสารประกอบเหล่านี้อธิบายคุณสมบัติทางเคมีของกรดอะมิโน ซึ่งคล้ายกับเอมีนและกรดคาร์บอกซิลิก ดังนั้นกรดอะมิโนจึงแสดงคุณสมบัติพื้นฐานของสารประกอบที่มีหมู่อะมิโนและคุณสมบัติที่เป็นกรดซึ่งเป็นลักษณะของสารประกอบที่มีหมู่คาร์บอกซิล ดังนั้นกรดอะมิโนจึงเป็นสารประกอบอินทรีย์แบบแอมโฟเทอริก
- ในการทำปฏิกิริยากับด่าง กรดอะมิโนจะแสดงคุณสมบัติเป็นกรด:
H 2 N-CH 2 -COOH + NaOH → H 2 N-CH 2 -COOH - นา ++น้ำ2O
- ในปฏิกิริยาเอสเทอริฟิเคชันกับแอลกอฮอล์ พวกมันยังแสดงคุณสมบัติที่เป็นกรดด้วย:
NH 2 CH 2 COOH + CH 3 OH → NH 2 CH 2 COOCH 3 + H 2 O
เมื่อทำปฏิกิริยากับกรดแก่จะมีคุณสมบัติพื้นฐานดังต่อไปนี้:
NH 2 CH 2 COOH + HCl → + Cl -
ปฏิกิริยากับกรดไนตรัสจะเกิดขึ้นเช่นเดียวกับในกรณีของเอมีนปฐมภูมิ:
NH 2 -CH 2 -COOH + HNO 2 → HO-CH 2 -COOH + N 2 + H 2 O
อัลคิเลชันของกรดอะมิโน:
NH 2 CH 2 COOH + CH 3 ฉัน → + ฉัน -
ในปฏิกิริยาระหว่างกัน กรดอะมิโนจะสร้างไดเปปไทด์ ซึ่งเป็นสารประกอบที่มีพันธะเปปไทด์ –C(O)-NH- ในโมเลกุลของพวกมัน ตัวอย่างเช่น ปฏิกิริยาของไกลซีนและอะลานีนทำให้เกิดไดเปปไทด์ไกลซิลาลานีน:
การทำปฏิกิริยานี้โดยไม่ปฏิบัติตามเงื่อนไขการสังเคราะห์ที่เฉพาะเจาะจงจะนำไปสู่การก่อตัวของอะลานิลไกลซีนมากกว่าไกลซิลาลานีน
| | |
เมื่อใช้บทเรียนวิดีโอนี้ ทุกคนจะได้แนวคิดในหัวข้อ “สารประกอบอินทรีย์ที่มีไนโตรเจน” ในวิดีโอนี้ คุณจะได้เรียนรู้เกี่ยวกับสารประกอบอินทรีย์ที่มีไนโตรเจน ครูจะพูดคุยเกี่ยวกับสารประกอบอินทรีย์ที่มีไนโตรเจน องค์ประกอบและคุณสมบัติของสารประกอบเหล่านั้น
หัวข้อ: อินทรียวัตถุ
บทเรียน: สารประกอบอินทรีย์ที่มีไนโตรเจน
สารประกอบอินทรีย์ธรรมชาติส่วนใหญ่มีไนโตรเจน เอ็น.เอช. 2 - กลุ่มอะมิโน สารอินทรีย์ที่มีโมเลกุลประกอบด้วย กลุ่มอะมิโน เรียกว่า เอมีน โครงสร้างของโมเลกุลเอมีนนั้นคล้ายคลึงกับโครงสร้างของแอมโมเนียดังนั้นคุณสมบัติของสารเหล่านี้จึงคล้ายกัน
เอมีนเป็นอนุพันธ์ของแอมโมเนียในโมเลกุลที่อะตอมไฮโดรเจนหนึ่งอะตอมหรือมากกว่านั้นถูกแทนที่ด้วยอนุมูลไฮโดรคาร์บอน สูตรทั่วไปของเอมีนคือ ร - เอ็น.เอช. 2.
ข้าว. 1. แบบจำลอง Ball-and-stick ของโมเลกุลเมทิลลามีน ()
หากแทนที่อะตอมไฮโดรเจนหนึ่งอะตอม เอมีนปฐมภูมิจะถูกสร้างขึ้น ตัวอย่างเช่น เมทิลลามีน
(ดูรูปที่ 1)
หากแทนที่ไฮโดรเจน 2 อะตอม จะเกิดเอมีนทุติยภูมิขึ้น ตัวอย่างเช่น ไดเมทิลลามีน
เมื่ออะตอมไฮโดรเจนทั้ง 3 อะตอมในแอมโมเนียถูกแทนที่ จะเกิดเอมีนตติยภูมิขึ้น ตัวอย่างเช่น ไตรเมทิลลามีน
ความหลากหลายของเอมีนนั้นพิจารณาจากจำนวนอะตอมไฮโดรเจนที่ถูกแทนที่เท่านั้น แต่ยังรวมถึงองค์ประกอบของอนุมูลไฮโดรคาร์บอนด้วย กับnเอช 2n +1 - เอ็นเอช 2เป็นสูตรทั่วไปสำหรับเอมีนปฐมภูมิ
คุณสมบัติของเอมีน
Methylamine, dimethylamine, trimethylamine เป็นก๊าซที่มีกลิ่นอันไม่พึงประสงค์ ว่ากันว่ามีกลิ่นคาว เนื่องจากมีพันธะไฮโดรเจน จึงสามารถละลายได้สูงในน้ำ แอลกอฮอล์ และอะซิโตน เนื่องจากพันธะไฮโดรเจนในโมเลกุลเมทิลลามีน จุดเดือดของเมทิลลามีน (bp = -6.3 ° C) จึงแตกต่างกันมากและมีเทนไฮโดรคาร์บอน CH 4 ที่สอดคล้องกัน (bp = -161.5 ° C) เอมีนที่เหลือจะเป็นของเหลวหรือของแข็งภายใต้สภาวะปกติ เป็นสารที่มีกลิ่นอันไม่พึงประสงค์ เอมีนที่สูงกว่าเท่านั้นจึงไม่มีกลิ่น ความสามารถของเอมีนในการทำปฏิกิริยาคล้ายกับแอมโมเนียก็เกิดจากการมีอิเล็กตรอนคู่ "โดดเดี่ยว" ในโมเลกุล (ดูรูปที่ 2)

ข้าว. 2. การมีอยู่ของอิเล็กตรอนคู่ "โดดเดี่ยว" ในไนโตรเจน
ปฏิสัมพันธ์กับน้ำ
สภาพแวดล้อมที่เป็นด่างในสารละลายที่เป็นน้ำของเมทิลลามีนสามารถตรวจพบได้โดยใช้ตัวบ่งชี้ เมทิลเอมีน ช 3 -เอ็นเอช 2- เป็นพื้นฐาน แต่เป็นประเภทอื่น คุณสมบัติหลักเกิดจากความสามารถของโมเลกุลในการยึดเกาะ H + แคตไอออน
สรุปโครงร่างปฏิสัมพันธ์ของเมทิลลามีนกับน้ำ:
ช 3 -เอ็นH 2 + H-OH → CH 3 -เอ็นชม 3 + + โอ้ -
เมทิลเอมีน เมทิล แอมโมเนียม ไอออน
ปฏิกิริยากับกรด
เอมีนทำปฏิกิริยากับกรดเช่นเดียวกับแอมโมเนีย ในกรณีนี้จะเกิดสารคล้ายเกลือที่เป็นของแข็ง
ค 2 ชั่วโมง 5 -เอ็นเอช 2 + เอ็นเอสล→ ค 2 ชั่วโมง 5 -เอ็นเอช 3 + + ซีล -
เอทิลเอมีน เอทิล แอมโมเนียม คลอไรด์
Ethylammonium chloride ละลายได้ดีในน้ำ สารละลายของสารนี้จะนำกระแสไฟฟ้า เมื่อเอทิลแอมโมเนียมคลอไรด์ทำปฏิกิริยากับอัลคาไล จะเกิดเอทิลลามีนขึ้น
ค 2 ชั่วโมง 5 -เอ็นเอช 3 + ซีล - + เอ็นaOH → C 2 H 5 -เอ็นฮ2+เอ็นอสล+ เอช 2 โอ
เมื่อเกิดการเผาไหม้เอมีนไม่เพียงแต่ก่อตัวเป็นคาร์บอนออกไซด์และน้ำเท่านั้น แต่ยังรวมถึงโมเลกุลด้วย ไนโตรเจน.
4CH 3 -เอ็นเอช 2 + 9O 2 → 4 CO 2 + 10 เอช 2 โอ + 2เอ็น 2
ส่วนผสมของเมทิลลามีนกับอากาศทำให้เกิดการระเบิดได้
เอมีนส่วนล่างใช้สำหรับการสังเคราะห์ยา ยาฆ่าแมลง และในการผลิตพลาสติกด้วย เมทิลลามีนเป็นสารประกอบที่เป็นพิษ มันทำให้เยื่อเมือกระคายเคือง กดการหายใจ และส่งผลเสียต่อระบบประสาทและอวัยวะภายใน
สรุปบทเรียน
คุณได้เรียนรู้สารอินทรีย์อีกประเภทหนึ่ง - เอมีน เอมีนเป็นสารประกอบอินทรีย์ที่มีไนโตรเจน หมู่ฟังก์ชันของเอมีนคือ NH 2 เรียกว่าหมู่อะมิโน เอมีนถือได้ว่าเป็นอนุพันธ์ของแอมโมเนียในโมเลกุลที่อะตอมไฮโดรเจนหนึ่งอะตอมหรือมากกว่านั้นถูกแทนที่ด้วยอนุมูลไฮโดรคาร์บอน เราตรวจสอบคุณสมบัติทางเคมีและกายภาพของเอมีน
1. Rudzitis G.E. เคมีอนินทรีย์และอินทรีย์ ชั้นประถมศึกษาปีที่ 9 หนังสือเรียนสถานศึกษาทั่วไป ระดับพื้นฐาน / G.E. Rudzitis, F.G. เฟลด์แมน. - อ.: การศึกษา, 2552.
2. โปเปล พี.พี. เคมี. ชั้นประถมศึกษาปีที่ 9 : หนังสือเรียนสำหรับสถานศึกษาทั่วไป / ป.ป. โปเปล, แอล.เอส. คริฟลียา. - K.: IC "Academy", 2552. - 248 หน้า: ป่วย.
3. กาเบรียลยัน โอ.เอส. เคมี. ชั้นประถมศึกษาปีที่ 9: หนังสือเรียน - อ.: อีแร้ง, 2544. - 224 น.
1. Rudzitis G.E. เคมีอนินทรีย์และอินทรีย์ ชั้นประถมศึกษาปีที่ 9 หนังสือเรียนสถานศึกษาทั่วไป ระดับพื้นฐาน / G.E. Rudzitis, F.G. เฟลด์แมน. - อ.: การศึกษา, 2552. - ฉบับที่ 13-15 (หน้า 173).
2. คำนวณเศษส่วนมวลของไนโตรเจนในเมทิลลามีน
3. เขียนปฏิกิริยาการเผาไหม้ของโพรพิลามีน ระบุผลรวมของสัมประสิทธิ์ของผลิตภัณฑ์ปฏิกิริยา
กรดอะมิโนเป็นองค์ประกอบโครงสร้างหลักของโมเลกุลโปรตีนและปรากฏอยู่ในรูปแบบอิสระในผลิตภัณฑ์อาหารในระหว่างกระบวนการสลายโปรตีน
กรดอะมิโนเอไมด์ที่มีอยู่ในผลิตภัณฑ์จากพืชที่เป็นส่วนประกอบตามธรรมชาติ ตัวอย่างเช่น กะหล่ำปลีและหน่อไม้ฝรั่งมีแอสพาราจีนเอไมด์ (0.2-0.3%)
สารประกอบแอมโมเนียพบในผลิตภัณฑ์อาหารในปริมาณเล็กน้อยในรูปของแอมโมเนียและอนุพันธ์ของมัน แอมโมเนียเป็นผลสุดท้ายของการสลายโปรตีน แอมโมเนียและเอมีนในปริมาณที่มีนัยสำคัญบ่งชี้ถึงการสลายตัวที่เน่าเปื่อยของโปรตีนในอาหาร ดังนั้นเมื่อศึกษาความสดของเนื้อสัตว์และปลาจึงพิจารณาปริมาณแอมโมเนียในนั้น อนุพันธ์ของแอมโมเนีย ได้แก่ โมโนเอมีน CH 3 NH 2, ไดเมทิลเอมีน (CH 3) 2 NH และไตรเมทิลเอมีน (CH 3) 3 N ซึ่งมีกลิ่นเฉพาะ เมทิลลามีนมีกลิ่นคล้ายแอมโมเนีย ไดเมทิลลามีนเป็นสารก๊าซที่มีกลิ่นของน้ำเกลือแฮร์ริ่งซึ่งส่วนใหญ่เกิดขึ้นระหว่างการเน่าเปื่อยของโปรตีนจากปลาและผลิตภัณฑ์อื่น ๆ Trimethylamine เป็นสารก๊าซที่มีอยู่ในน้ำเกลือปลาเฮอริ่งในปริมาณมาก ในรูปแบบเข้มข้นจะมีกลิ่นแอมโมเนีย แต่ในระดับความเข้มข้นต่ำจะมีกลิ่นของปลาเน่า
ไนเตรต- เกลือของกรดไนตริก พบได้ในผลิตภัณฑ์อาหารในปริมาณเล็กน้อย ยกเว้นฟักทองและบวบ
ไนไตรต์เติมในปริมาณเล็กน้อยเมื่อเกลือเนื้อและไส้กรอกสับเพื่อให้เนื้อมีสีชมพู ไนไตรต์มีความเป็นพิษสูง ดังนั้นการใช้ในอุตสาหกรรมอาหารจึงมีจำกัด (เติมสารละลายไนไตรต์ลงในเนื้อสับในอัตราไม่เกิน 0.005% ของมวลเนื้อสัตว์)
กระรอกเป็นสารประกอบที่มีไนโตรเจนที่สำคัญที่สุดสำหรับโภชนาการของมนุษย์ เป็นสารประกอบอินทรีย์ที่สำคัญที่สุดที่พบในสิ่งมีชีวิต ย้อนกลับไปในช่วงศตวรรษที่ผ่านมา ขณะศึกษาองค์ประกอบของสัตว์และพืชหลายชนิด นักวิทยาศาสตร์ได้แยกสารที่มีคุณสมบัติบางอย่างคล้ายกับไข่ขาว ตัวอย่างเช่น พวกมันจับตัวเป็นก้อนเมื่อถูกความร้อน สิ่งนี้ทำให้เกิดการเรียกพวกมันว่าโปรตีน F. Engels ตั้งข้อสังเกตถึงความสำคัญของโปรตีนที่เป็นพื้นฐานของสิ่งมีชีวิตทั้งหมด เขาเขียนว่าที่ใดมีชีวิต โปรตีนจะถูกพบ และที่ใดมีโปรตีน ที่นั่นย่อมมีสัญญาณแห่งชีวิต
ดังนั้น คำว่า "โปรตีน" จึงหมายถึงสารประกอบอินทรีย์โมเลกุลสูงที่มีไนโตรเจนสูงหลายประเภทที่มีอยู่ในทุกเซลล์และเป็นตัวกำหนดกิจกรรมที่สำคัญของมัน
องค์ประกอบทางเคมีของโปรตีน การวิเคราะห์ทางเคมีแสดงให้เห็นว่ามีโปรตีนทั้งหมด (เป็น%): คาร์บอน - 50-55, ไฮโดรเจน - 6-7, ออกซิเจน - 21-23, ไนโตรเจน - 15-17, ซัลเฟอร์ - 0.3-2.5 พบฟอสฟอรัส ไอโอดีน เหล็ก ทองแดง และธาตุมาโครและจุลธาตุบางชนิดในปริมาณที่แตกต่างกันในโปรตีนแต่ละชนิด
เพื่อตรวจสอบลักษณะทางเคมีของโมโนเมอร์โปรตีน จะดำเนินการไฮโดรไลซิส - การต้มโปรตีนเป็นเวลานานด้วยกรดหรือเบสแร่ที่แข็งแกร่ง ที่ใช้กันมากที่สุดคือ 6N HN0 3 และเดือดที่ 110°C เป็นเวลา 24 ชั่วโมง ในระยะต่อไป สารที่รวมอยู่ในไฮโดรไลเสตจะถูกแยกออกจากกัน เพื่อจุดประสงค์นี้จึงใช้วิธีโครมาโตกราฟี ในที่สุดธรรมชาติของโมโนเมอร์ที่แยกได้จะถูกทำให้กระจ่างขึ้นโดยใช้ปฏิกิริยาเคมีบางอย่าง พบว่าส่วนประกอบเริ่มต้นของโปรตีนคือกรดอะมิโน
น้ำหนักโมเลกุล (มม.) ของโปรตีนอยู่ระหว่าง 6,000 ถึง 1,000,000 และสูงกว่า ดังนั้น mm โปรตีนอัลบูมินนม - 17400, โกลบูลินนม - 35200, อัลบูมินไข่ - 45000 ในร่างกายของสัตว์และพืชโปรตีนพบได้ในสามสถานะ: ของเหลว (นม, เลือด), น้ำเชื่อม (ไข่ขาว) และของแข็ง (ผิวหนัง, ผม, ขนสัตว์).
ขอบคุณ M.M. ขนาดใหญ่ โปรตีนอยู่ในสถานะคอลลอยด์และกระจายตัว (กระจาย, กระจัดกระจาย, แขวนลอย) ในตัวทำละลาย โปรตีนส่วนใหญ่เป็นสารประกอบที่ชอบน้ำซึ่งมีความสามารถในการทำปฏิกิริยากับน้ำซึ่งจับกับโปรตีน ปฏิกิริยานี้เรียกว่าการให้ความชุ่มชื้น
โปรตีนหลายชนิดภายใต้อิทธิพลของปัจจัยทางกายภาพและเคมีบางอย่าง (อุณหภูมิ ตัวทำละลายอินทรีย์ กรด เกลือ) จับตัวเป็นก้อนและตกตะกอน กระบวนการนี้เรียกว่าการสูญเสียสภาพธรรมชาติ โปรตีนที่ถูกทำลายจะสูญเสียความสามารถในการละลายในน้ำ สารละลายเกลือ หรือแอลกอฮอล์ อาหารทุกชนิดที่ผ่านกระบวนการที่อุณหภูมิสูงจะมีโปรตีนที่ถูกทำลาย สำหรับโปรตีนส่วนใหญ่ อุณหภูมิในการสลายตัวคือ 50-60 °C ความสามารถของโปรตีนในการสลายตัวเป็นสิ่งสำคัญ โดยเฉพาะอย่างยิ่งเมื่ออบขนมปังและผลิตผลิตภัณฑ์ขนม คุณสมบัติที่สำคัญอย่างหนึ่งของโปรตีนคือความสามารถในการสร้างเจลเมื่อบวมในน้ำ การบวมของโปรตีนมีความสำคัญอย่างยิ่งในการผลิตขนมปัง พาสต้า และผลิตภัณฑ์อื่นๆ เมื่อเจลมีอายุมากขึ้น เจลจะสูญเสียน้ำ ปริมาณและริ้วรอยลดลง ปรากฏการณ์นี้ซึ่งตรงกันข้ามกับอาการบวม เรียกว่าซินเนอริซิส
หากจัดเก็บผลิตภัณฑ์โปรตีนอย่างไม่เหมาะสม อาจเกิดการสลายตัวของโปรตีนในระดับลึกยิ่งขึ้นเมื่อมีการปล่อยผลิตภัณฑ์ที่สลายตัวของกรดอะมิโน รวมถึงแอมโมเนียและคาร์บอนไดออกไซด์ โปรตีนที่มีซัลเฟอร์จะปล่อยไฮโดรเจนซัลไฟด์ออกมา
บุคคลต้องการโปรตีน 80-100 กรัมต่อวัน รวมทั้งโปรตีนจากสัตว์ 50 กรัมด้วย เมื่อโปรตีน 1 กรัมถูกออกซิไดซ์ ร่างกายจะปล่อยพลังงานออกมา 16.7 กิโลจูล หรือ 4.0 กิโลแคลอรี
กรดอะมิโน -เหล่านี้เป็นกรดอินทรีย์ซึ่งอะตอมไฮโดรเจนของอะตอม oc-คาร์บอนถูกแทนที่ด้วยกลุ่มอะมิโน NH 2 ดังนั้นจึงเป็นกรด oc-amino ที่มีสูตรทั่วไป
ควรสังเกตว่ากรดอะมิโนทั้งหมดมีกลุ่มร่วมกัน: - CH 2, -NH 2, -COOH และสายด้านข้างของกรดอะมิโนหรืออนุมูล (R) แตกต่างกัน ลักษณะทางเคมีของอนุมูลมีความหลากหลาย ตั้งแต่อะตอมไฮโดรเจนไปจนถึงสารประกอบไซคลิก เป็นอนุมูลที่กำหนดลักษณะโครงสร้างและหน้าที่ของกรดอะมิโน
กรดอะมิโนในสารละลายที่เป็นน้ำอยู่ในสถานะแตกตัวเป็นไอออนเนื่องจากการแตกตัวของหมู่เอมีนและคาร์บอกซิล รวมถึงหมู่ที่เป็นส่วนหนึ่งของอนุมูล กล่าวอีกนัยหนึ่ง พวกมันเป็นสารประกอบแอมโฟเทอร์มิกและสามารถมีอยู่ได้ทั้งในรูปแบบกรด (ผู้ให้โปรตอน) หรือเบส (ตัวรับโปรตอน)
กรดอะมิโนทั้งหมดแบ่งออกเป็นหลายกลุ่มขึ้นอยู่กับโครงสร้างของพวกมัน

จากกรดอะมิโน 20 ชนิดที่เกี่ยวข้องกับการสร้างโปรตีน กรดอะมิโนบางชนิดไม่ได้มีคุณค่าทางชีวภาพเหมือนกันทั้งหมด กรดอะมิโนบางชนิดถูกสังเคราะห์โดยร่างกายมนุษย์ และความต้องการกรดอะมิโนเหล่านี้ก็ได้รับการตอบสนองโดยไม่ต้องจ่ายจากภายนอก กรดอะมิโนดังกล่าวเรียกว่าไม่จำเป็น (ฮิสติดีน, อาร์จินีน, ซีสตีน, ไทโรซีน, อะลานีน, ซีรีส์, กรดกลูตามิกและแอสปาร์ติก, โพรลีน, ไฮดรอกซีโพรลีน, ไกลซีน) กรดอะมิโนที่เหลือไม่ได้ถูกสังเคราะห์โดยร่างกายและจะต้องได้รับจากอาหาร พวกเขาเรียกว่าจำเป็น (ทริปโตเฟน) โปรตีนที่มีกรดอะมิโนจำเป็นทั้งหมดเรียกว่าโปรตีนสมบูรณ์ และหากไม่มีกรดจำเป็นอย่างน้อยหนึ่งตัว โปรตีนก็จะไม่สมบูรณ์
การจำแนกประเภทของโปรตีน การจำแนกประเภทของโปรตีนขึ้นอยู่กับลักษณะทางเคมีกายภาพและเคมี โปรตีนแบ่งออกเป็นแบบง่าย (โปรตีน) และเชิงซ้อน (โปรตีน) โปรตีนเชิงเดี่ยวรวมถึงโปรตีนที่เมื่อไฮโดรไลซิสจะให้กรดอะมิโนเท่านั้น โปรตีนเชิงซ้อนคือโปรตีนที่ประกอบด้วยโปรตีนเชิงเดี่ยวและสารประกอบของกลุ่มที่ไม่ใช่โปรตีนที่เรียกว่าอวัยวะเทียม
โปรตีนได้แก่ อัลบูมิน (นม ไข่ เลือด) โกลบูลิน (ไฟบริโนเจนในเลือด ไมโอซินของเนื้อ โกลบูลินไข่ ทูเบอรินมันฝรั่ง ฯลฯ) กลูเทลิน (ข้าวสาลีและข้าวไรย์) โพรดามิน (ไกลาดินของข้าวสาลี) สคลีโอโปรตีน (คอลลาเจนของกระดูก ผ้าอีลาสตินที่เกี่ยวพัน) ,เคราตินผม)
โปรตีน ได้แก่ ฟอสโฟโปรตีน (เคซีนนม ไวเทลลินไข่ไก่ ไข่ปลาอิชทูลิน) ซึ่งประกอบด้วยโปรตีนและกรดฟอสฟอริก โครโมโปรตีน (ฮีโมโกลบินในเลือด, เนื้อเยื่อกล้ามเนื้อเนื้อไมโอโกลบิน) ซึ่งเป็นสารประกอบของโปรตีนโกลบินและสีย้อม glucolroteids (โปรตีนของกระดูกอ่อน, เยื่อเมือก) ประกอบด้วยโปรตีนและกลูโคสอย่างง่าย ไลโปโปรตีน (โปรตีนที่มีฟอสฟาไทด์) เป็นส่วนหนึ่งของโปรโตพลาสซึมและเมล็ดคลอโรฟิลล์ นิวคลีโอโปรตีนประกอบด้วยกรดนิวคลีอิกและมีบทบาทสำคัญทางชีวภาพต่อร่างกาย